题目内容
25℃时,在1.0 L浓度均为0.01 mol·L-1的某一元酸HA与其钠盐组成的混合溶液中,测得
c(Na+)>c(A-),则下列描述中,不正确的是( )
A.该溶液的pH<7
B.HA的酸性很弱,A-水解程度较大
C.c(A-)+c(HA)=0.02 mol·L-1
D.n(A-)+n(OH-)=0.01 mo1+n(H+)
A
解析试题分析:由c(Na+)>c(A-)得:在等浓度一元酸HA与其钠盐组成的混合溶液中,酸根离子水解程度大于酸的电离程度,所以溶液显碱性。A、该溶液的pH>7,错误;B、由以上分析知,正确;C、根据物料守恒,得c(A-)+c(HA)=0.02 mol·L-1,正确;D、根据电荷守恒,所以n(A-)+n(OH-)=n(Na+)+n(H+),其中n(Na+)=0.01mol,n(A-)+n(OH-)=0.01 mo1+n(H+),正确,答案选A。
考点:考查混合液中水解与电离程度的判断,物料守恒、电荷守恒规律的应用

练习册系列答案
相关题目
某浓度的氨水中存在下列平衡:NH3·H2O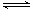 NH4+ + OH-,如想增大NH4+的浓度,而不增大OH-的浓度,应采取的措施是( )
NH4+ + OH-,如想增大NH4+的浓度,而不增大OH-的浓度,应采取的措施是( )
| A.适当升高温度 | B.加入水 | C.通入NH3 | D.加入少量盐酸 |
25 ℃时,水的电离达到平衡:H2O H++OH-,下列叙述中正确的是( )
H++OH-,下列叙述中正确的是( )
| A.将纯水加热到95 ℃时,KW变大,pH不变,水仍呈中性 |
| B.向纯水中加入稀氨水,平衡逆向移动,c(OH-)增大,KW变小 |
| C.向纯水中加入少量固体碳酸钠,c(H+)减小,KW不变,影响水的电离平衡 |
| D.向纯水中加入醋酸钠或盐酸,均可抑制水的电离,KW不变 |
下列解释实验事实的平衡不正确的是
| | 实 验 | 解释 |
| A | 100℃ 0.1 mol/LNa2SO4溶液pH= 6.2 | H2O H+ + OH- H+ + OH- |
| B | 0.1 mol/L CH3COOH的pH=3 | CH3COOH CH3COO- + H+ CH3COO- + H+ |
| C | 配制FeCl3溶液时加少量盐酸 | Fe3+ + 3OH- Fe(OH)3 Fe(OH)3 |
| D | 用稀硫酸洗涤BaSO4,沉淀损失小 | BaSO4(s)  Ba2+(aq) + SO42-(aq) Ba2+(aq) + SO42-(aq) |
下列水溶液一定呈中性的是( )
| A.c(NH4+)=c(Cl-)的NH4Cl溶液 |
| B.c(H+)=1.0×10-7 mol·L-1的溶液 |
| C.pH=7的溶液 |
| D.室温下将pH=3的酸与pH=11的碱等体积混合后的溶液 |
现有室温下的四种溶液,有关叙述不正确的是
| 编号 | ① | ② | ③ | ④ |
| pH | 11 | 11 | 3 | 3 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸溶液 | 盐酸 |
A.相同体积的③、④溶液分别与NaOH完全反应,消耗NaOH的物质的量:③>④
B.分别加水稀释10倍,四种溶液的pH:①>②>④>③
C.①、④两溶液等体积混合,所得溶液中:c(Cl-)>c(
 )>c(OH-)>c(H+)
)>c(OH-)>c(H+)D.Va L④溶液与Vb L②溶液混合[近似认为混合溶液体积=(Va+Vb)L],若混合后溶液的pH=4,则Va∶Vb=11∶9
下列说法中正确的是( )
| A.在Na2CO3溶液中滴入酚酞试液,呈红色 |
B.(NH4)2SO4溶液中c(NH )∶c(SO )∶c(SO )=2∶1 )=2∶1 |
| C.FeCl3溶于水使溶液呈酸性,从而抑制水的电离 |
| D.将Al2(SO4)3溶液蒸干得到Al(OH)3固体 |
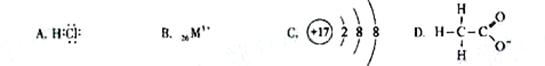
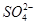 )
)