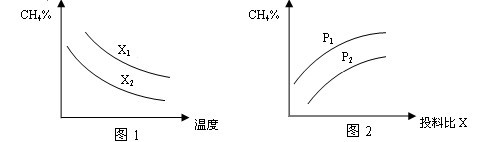
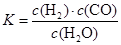��Ŀ����
����β���к���CO��NO2���ж����壬��������װβ������װ�ã���ʹ�ж��������Ӧת��Ϊ�����塣
��1������β����CO��NO2������һ�������¿��Է�����Ӧ��
4CO(g)+2NO2(g) 4CO2(g)+N2(g)����H=��1200 kJ��mol��1
4CO2(g)+N2(g)����H=��1200 kJ��mol��1
�ٺ��º��������£�����˵���÷�Ӧ�Ѵﵽƽ��״̬����________(�����)��
A�������ڻ��������ɫ���ٱ仯 B�������ڵ�ѹǿ���ֲ���
C��2v��(NO2)=v��(N2) D�������ڻ�������ܶȱ��ֲ���
����ʹ�÷�Ӧ�ķ�Ӧ����������ƽ�����淴Ӧ�����ƶ�����________(�����)��
A����ʱ�����CO2 B���ʵ������¶�
C����С�������ʹ��ϵѹǿ���� D��ѡ���Ч����
�۶��ڸ÷�Ӧ���¶Ȳ�ͬ(T2>T1)������������ͬʱ������ͼ����ȷ����________(�����)��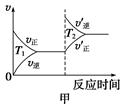
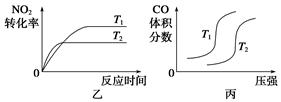
��2������β����CO��H2O(g)��һ�������¿��Է�����Ӧ��CO(g)+H2O(g) CO2(g)+H2(g) ��H<0��820 ��ʱ�ڼס��ҡ������������ܱ������У���ʼʱ�����ұ�����Ͷ�ϣ��ﵽƽ��״̬ʱK=1.0��
CO2(g)+H2(g) ��H<0��820 ��ʱ�ڼס��ҡ������������ܱ������У���ʼʱ�����ұ�����Ͷ�ϣ��ﵽƽ��״̬ʱK=1.0��
| ��ʼ���ʵ��� | �� | �� | �� |
| n(H2O)/mol | 0.10 | 0.20 | 0.20 |
| n(CO)/mol | 0.10 | 0.10 | 0.20 |
�ٸ÷�Ӧ��ƽ�ⳣ������ʽΪ___________��ƽ��ʱ����������CO��ת����= ��
��ƽ��ʱ���Ƚ�����������CO��ת���ʣ��� ��(�>������=����<������ͬ)���� �ס�
��15�֣�
��1�� �� C D�� �� B �� �ң���2�֣�
��2�� ��K=" c" (CO2)��c (H2)��[c (CO)��c (H2O)]��2�֣� 50% ��3�֣�
�ڡ�> = ����2�֣���
���������������1���ٷ�Ӧ��ϵ��ֻ�ж��������Ǻ���ɫ���壬�����Ϊ��ɫ���壬������������ɫ���ٱ仯��˵����������Ũ�Ȳ��ٱ仯������Ӧ�ﵽƽ�⣬��A��������Ӧ������У���������Ӧ���������ʵ�����С�ķ�Ӧ����������ڻ�������ѹǿ��С����ѹǿ���ֲ��䣬˵������ֵ����ʵ������ֲ��䣬����Ӧ�ﵽƽ�⣬��B����ͬһ���ʱ�ʾ��v��= v������ͬ���ʱ�ʾ�淴Ӧ���ʺ�����Ӧ����֮�ȵ��ڻ�ѧ����ʽ�ж�Ӧϵ��֮�ȣ�����˵����Ӧ�ﵽƽ�⣬��v��(NO2)/v��(N2)=2/1������v��(NO2)=2v��(N2)��˵����Ӧ�ﵽƽ�⣬��2v��(NO2)=v��(N2)����˵����Ӧ�ﵽƽ�⣬��C��ȷ�����������ܶȵ������������������ݻ������ڷ�Ӧ��������ﶼ�����壬��Ӧ��ѭ�����غ㶨�ɣ���������������ʼ�ղ��䣬����������������䣬����������ܶ�ʼ�ղ���ı䣬����ܶȲ��䲻��˵����Ӧ�ﵽƽ�⣬��D��ȷ���ڼ�ʱ�����������̼������С������Ũ�ȣ���Ӧ���ʼ�С��ƽ��������Ӧ�����ƶ�����A����H=��1200 kJ��mol��1��������Ӧ�Ƿ��ȷ�Ӧ�������¶ȣ���Ӧ��������ƽ�������ȷ�Ӧ���淴Ӧ�����ƶ�����B��ȷ������Ӧ�����������С�ķ���С�����������ѹǿ������Ӧ���������Ũ�ȣ���Ӧ��������ƽ�������������С������Ӧ�����ƶ�����C����ѡ���Ч������������Ӧ���ʣ����Ƕ�ƽ����Ӱ�죬ƽ�ⲻ�ƶ�����D����ƽ��ʱ�����¶ȣ����淴Ӧ���ʶ���ͻȻ���������ȷ�Ӧ�������������̶ȴ��ڷ��ȷ�Ӧ��������ʣ����淴Ӧ����>����Ӧ����>ԭƽ��ʱ�����淴Ӧ����=ԭƽ��ʱ���淴Ӧ���ʣ��ʼ�ͼ���������¶ȣ���Ӧ���ʼӿ죬ƽ�����淴Ӧ�����ƶ����������̴ﵽƽ���ʱ�䣬����ʹ��Ӧ���ƽ��ת���ʼ�С����T2ʱ���߱�T1ʱ�ȴﵽƽ�⣬ƽ��ʱ����������ת���ʽ��ͣ�����ͼ��ȷ������ѹǿ��ƽ��������Ӧ�����ƶ�����Ӧ������ʵ�����С����һ����̼�����������С���������������¶ȣ�ƽ�����淴Ӧ�����ƶ�����Ӧ������ʵ���������һ����̼��������������Ǽ�С���ʱ�ͼ����2����ƽ�ⳣ������ƽ��ʱ������Ũ����֮���뷴Ӧ��Ũ����֮���ı�ֵ����CO(g)+H2O(g) CO2(g)+H2(g)��ƽ�ⳣ��K�ı���ʽΪ
CO2(g)+H2(g)��ƽ�ⳣ��K�ı���ʽΪ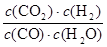 �����������ݻ�δ֪��Ϊ�˼�������̣������ݻ�Ϊ1L����������CO�ı仯Ũ��Ϊx mol��L��1������÷�Ӧ�и���ֵģ���ʼ���仯��ƽ�⣩Ũ�ȣ���
�����������ݻ�δ֪��Ϊ�˼�������̣������ݻ�Ϊ1L����������CO�ı仯Ũ��Ϊx mol��L��1������÷�Ӧ�и���ֵģ���ʼ���仯��ƽ�⣩Ũ�ȣ���
CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
��ʼŨ��/mol��L��1 0.10 0.10 0 0
�仯Ũ��/mol��L��1 x x x x
ƽ��Ũ��/mol��L��1 0.10��x 0.10��x x x
K=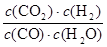 =
=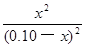 =1.0
=1.0
��ã�x =0.050
��1���ס��ң���������ˮ������Ũ�ȣ�����һ�ַ�Ӧ��Ũ�ȣ�ƽ��������Ӧ�����ƶ�����һ�ַ�Ӧ���ת����������һ����̼��ƽ��ת���ʣ���<�ң�����ͨ������Ƚϣ���
�����ݻ�Ϊ1L����������CO�ı仯Ũ��Ϊy mol��L��1������÷�Ӧ�и���ֵģ���ʼ���仯��ƽ�⣩Ũ�ȣ���
CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
��ʼŨ��/mol��L��1 0.10 0.20 0 0
�仯Ũ��/mol��L��1 y y y y
ƽ��Ũ��/mol��L��1 0.10��y 0.20��y y y
K=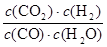 =
=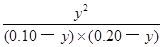 =1.0
=1.0
��ã�y =0.20/3
��ƽ��ʱ��������һ����̼��ƽ��ת����Ϊ��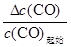 ��100%=
��100%=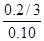 ��100%=67%>50%��
��100%=67%>50%��
2���ס�������ʼͶ�ϼӱ���Ͷ�ϱȲ��䣬�����������ַ�Ӧ��Ũ������ѹǿ����������Ӧ�������������ķ�Ӧ����ƽ�ⲻ�ƶ���һ����̼ƽ��ת���ʱ��ֲ��䣬��һ����̼��ƽ��ת���ʣ���=��������ͨ������Ƚϣ���
�����ݻ�Ϊ1L����������CO�ı仯Ũ��Ϊz mol��L��1������÷�Ӧ�и���ֵģ���ʼ���仯��ƽ�⣩Ũ�ȣ���
CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
��ʼŨ��/mol��L��1 0.20 0.20 0 0
�仯Ũ��/mol��L��1 z z z z
ƽ��Ũ��/mol��L��1 0.20��z 0.20��z z z
K=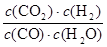 =
=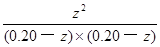 =1.0
=1.0
��ã�z =0.10
��ƽ��ʱ��������һ����̼��ƽ��ת����Ϊ��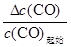 ��100%=
��100%=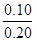 ��100%=50%��
��100%=50%��
���㣺���黯ѧ��Ӧԭ�����漰��ѧƽ����ж����ݡ���������Ի�ѧ��Ӧ���ʺ�ƽ���ƶ���Ӱ�졢��ѧ��Ӧ���ʺͻ�ѧƽ��ͼ��ƽ�ⳣ������ʽ����ѧƽ�ⳣ����ƽ��ת���ʵļ���ȡ�

��16�֣������еIJ��ֵ�Դ��O3�Ժ�ˮ��I������������O3����ͨ��NaI��Һ�н���ģ���о���
��1��O3��I��������I2�Ĺ�����3����Ӧ��ɣ�
��I��(aq)+ O3(g)==IO��(aq)+O2(g) ��H1
��IO��(aq)+H+(aq)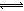 HOI(aq) ��H2
HOI(aq) ��H2
��HOI(aq)+ I��(aq)+ H+(aq)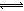 I2(aq)+H2O(l) ��H3
I2(aq)+H2O(l) ��H3
�ܷ�Ӧ�Ļ�ѧ����ʽΪ______���䷴Ӧ��H=______��
��2������Һ�д��ڻ�ѧƽ�⣺I2(aq)+I��(aq)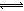 I3��(aq)����ƽ�ⳣ������ʽΪ_______��
I3��(aq)����ƽ�ⳣ������ʽΪ_______��
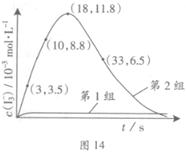
��3��Ϊ̽��Fe2+������I����Ӧ��Ӱ�죨��Ӧ��ϵ��ͼ13����ij�о�С��ⶨ����ʵ����I3��Ũ�Ⱥ���ϵpH�������ͼ14���±���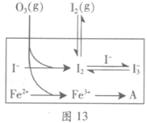
| ��� | ��Ӧ�� | ��ӦǰpH | ��Ӧ��pH |
| ��1�� | O3+ I�� | 5.2 | 11.0 |
| ��2�� | O3+ I��+ Fe2+ | 5.2 | 4.1 |
��ͼ13�е�AΪ ����Fe3+����A�Ĺ������������I����ת���ʣ�ԭ����_______��
�۵�2��ʵ�����18s��I3���½��������½���ֱ��ԭ���У�˫ѡ��______��
A��c(H+)��С B��c(I��)��С C��I2(g)�������� D��c(Fe3+)����
��4����ͼ14������3��18s�ڵ�2��ʵ��������I3����ƽ����Ӧ���ʣ�д��������̣����������λ��Ч���֣���
ijС������H2C2O4��Һ������KMnO4��Һ��Ӧ��̽���������Ի�ѧ��Ӧ���ʵ�Ӱ�족��ʵ��ʱ���ȷֱ���ȡ������Һ��Ȼ�����Թ���Ѹ����Ͼ��ȣ���ʼ��ʱ��ͨ���ⶨ��ɫ����ʱ�����жϷ�Ӧ�Ŀ�������С����������µķ�����
| ��� | H2C2O4��Һ | ����KMnO4��Һ | �¶�/�� | ||
| Ũ��/ mol?L��1 | ���/mL | Ũ��/ mol?L��1 | ���/mL | ||
| �� | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
| �� | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
| �� | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
��1����֪��Ӧ��H2C2O4ת��ΪCO2�ݳ���KMnO4ת��ΪMnSO4��ÿ����1mol H2C2O4ת��_____mol ���ӡ�Ϊ�˹۲쵽��ɫ��ȥ��H2C2O4��KMnO4��ʼ�����ʵ�����Ҫ����Ĺ�ϵΪ��c(H2C2O4)��c(KMnO4) ��______________��
��2��̽���¶ȶԻ�ѧ��Ӧ����Ӱ���ʵ������___________�����ţ���ͬ������̽����Ӧ��Ũ�ȶԻ�ѧ��Ӧ����Ӱ���ʵ������_____________��
��3��ʵ��ٲ��KMnO4��Һ����ɫʱ��Ϊ40s�����Ի��ǰ����Һ�����С�仯�����ʱ����ƽ����Ӧ����v��KMnO4��=_______________ mol?L��1?min��1��
��4����֪50��ʱc(MnO4��)����Ӧʱ��t�ı仯������ͼ�������������������䣬���ڴ������ͼ�У�����25��ʱc(MnO4��)��t�ı仯����ʾ��ͼ��

��7�֣�Ϊ���о���������Թ�������ֽ����ʵ�Ӱ�죬ijͬѧ��������ʵ�飺
| ��� | ���� | ʵ������ |
| �� | �ֱ����Թ�A��B�м���5 mL 5% H2O2��Һ��������2��1 mol��L��1 FeCl3��Һ�����Թ��о����������ݳ���ʱ�����Թ�A����ʢ��5��������ˮ���ձ��н��ݣ����Թ�B����ʢ��40��������ˮ���ձ��н��� | �Թ�A�����������ݲ����� �Թ�B�в��������������� |
| �� | ��ȡ��֧�Թֱܷ����5 mL 5% H2O2��Һ��5 mL 10% H2O2��Һ | �Թ�A��B�о�δ���Լ��������ݲ��� |
��1����������ֽ�Ļ�ѧ����ʽΪ �������������� ��
��2��ʵ��ٵ�Ŀ����___________________________________________________��ʵ���еμ�FeCl3��Һ��Ŀ����________________________________________��
��3��ʵ���δ�۲쵽Ԥ�ڵ�ʵ������Ϊ�˰�����ͬѧ�ﵽʵ��Ŀ�ģ�������Ķ����������ĸĽ������_________________________����ʵ�������ṩ���Լ�����������
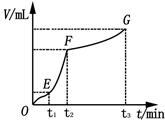
��4��ijͬѧ��50 mLһ��Ũ�ȵ�H2O2��Һ�м���һ�����Ķ������̣��ų�������������״���£��뷴Ӧʱ��Ĺ�ϵ����ͼ��ʾ�������ж�OE��EF��FG�����У�___________�λ�ѧ��Ӧ������졣
�����й��к͵ζ��IJ��������ñ�Һ��ϴ�ζ��ܣ������ζ�����ע�����Һ���ۼ��ζ����Ƿ�©ˮ���ܵζ����ݵμ�ָʾ���ڴ���Һ����ϴ�ӡ���ȷ�IJ���˳����
| A���ޢۢ٢ڢݢ� | B���ݢ٢ڢޢܢ� | C���ݢܢۢڢ٢� | D���ۢ٢ڢܢݢ� |
 2C�ﵽƽ�⡣���ⶨ��ƽ��ʱc(A2)=0.5mol/L��c(B2)=0.1mol/L��c(C)=1.6mol/L����A2��B2��C����ʼŨ�ȷֱ�Ϊamol/L��bmol/L��cmol/L��
2C�ﵽƽ�⡣���ⶨ��ƽ��ʱc(A2)=0.5mol/L��c(B2)=0.1mol/L��c(C)=1.6mol/L����A2��B2��C����ʼŨ�ȷֱ�Ϊamol/L��bmol/L��cmol/L��