题目内容
某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“条件对化学反应速率的影响”。实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢。该小组设计了如下的方案。
| 编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度/℃ | ||
| 浓度/ mol?L-1 | 体积/mL | 浓度/ mol?L-1 | 体积/mL | ||
| ① | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
| ② | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
| ③ | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
(1)已知反应后H2C2O4转化为CO2逸出,KMnO4转化为MnSO4,每消耗1mol H2C2O4转移_____mol 电子。为了观察到紫色褪去,H2C2O4与KMnO4初始的物质的量需要满足的关系为:c(H2C2O4)∶c(KMnO4) ≥______________。
(2)探究温度对化学反应速率影响的实验编号是___________(填编号,下同),可探究反应物浓度对化学反应速率影响的实验编号是_____________。
(3)实验①测得KMnO4溶液的褪色时间为40s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(KMnO4)=_______________ mol?L-1?min-1。
(4)已知50℃时c(MnO4-)~反应时间t的变化曲线如图。若保持其他条件不变,请在答题卡坐标图中,画出25℃时c(MnO4-)~t的变化曲线示意图。

(16分)(1)2 2.5(每空3分)
(2)②和③ ①和②(每空2分)
(3)0.010或1.0 ×10-2(3分,0.01得2分)
(4)如图(3分。标注1分,正确做图2分)
解析试题分析:(1)草酸中碳元素为+3价,二氧化碳中碳元素为+4价,由化合价升高总数等于转移电子数可知1个H2C2O4转移2个电子,则每消耗1molH2C2O4转移2mol 电子;草酸与酸性高锰酸钾溶液反应为5H2C2O4+2KMnO4+3H2SO4=10CO2↑+K2SO4+2MnSO4+8H2O~10e-,只有当KMnO4完全反应,溶液的紫红色才能褪去,如果n(H2C2O4)=5mol、n(KMnO4)≤2mol,就能观察到紫色褪去,所以c(H2C2O4)∶c(KMnO4) = n(H2C2O4)∶n(KMnO4)≥2.5;(2)根据控制变量设计探究实验方案原则,实验②和③所用试剂的浓度、体积均相同,反应温度分别为25℃、50℃,这组对比实验的目的是探究温度对化学反应速率的影响;实验①和②的温度相同,酸性高锰酸钾溶液的浓度、体积均相同,草酸浓度分别为0.1mol/L、0.2mol/L,这组实验的目的是探究浓度对化学反应速率的影响;实验①和③既改变了反应物的浓度,又改变了反应温度,不能得到合理的结论;(3)实验①中:2.0mL草酸溶液加入4.0mL酸性高锰酸钾溶液,能稀释后者,设稀释后高锰酸钾的初始浓度为xmol/L,根据题意和稀释定律(c1?V1=c2?V2)可知,0.010 mol?L-1×4.0×10-3L=x mol?L-1×(4.0+2.0)×10-3L,则x=0.010 mol?L-1×4.0/6.0,紫色恰好褪色时高锰酸钾浓度减小为0,则△c(KMnO4) =0.010 mol?L-1×4.0/6.0,而△t=40/60min,由v=△c/△t可得,v(KMnO4)=△c(KMnO4)/△t=0.010 mol?L-1×4.0/6.0÷40/60min=0.010 mol?L-1?min-1;(4)根据控制变量原则,高锰酸根离子的起始浓度不变,仅仅降低温度,反应速率减小,则褪色的时间增大,相同时间内高锰酸根离子的变化浓度减小,则25℃时反应过程中c(MnO4-)~t的变化曲线位于50℃时曲线的右边。
考点:考查氧化还原反应、浓度和温度对化学反应速率的影响、稀释定律、物质的量浓度和平均反应速率的计算、画出不同温度对反应物浓度与反应时间的变化示意图等。

 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案工业上以氨气为原料(铂铑合金网为催化剂)催化氧化法制硝酸的过程如下:
|

 (1)己知反应一经发生,铂铑合金网就会处于红热状态。写出氨催化氧化的化学方程式:______________________________________________;当温度升高时,该反应的平衡常数K值___________(填“增大”、“减小”或“不变”)。
(1)己知反应一经发生,铂铑合金网就会处于红热状态。写出氨催化氧化的化学方程式:______________________________________________;当温度升高时,该反应的平衡常数K值___________(填“增大”、“减小”或“不变”)。(2)硝酸厂尾气常用的处理方法是催化还原法:催化剂存在时用H2将NO2还原为N2。已知:
2H2(g)+O2(g)=2H2O(g) △H= a kJ·mol-1
N2(g)+2O2(g)=2NO2(g) △H= b kJ·mol-1
H2O(1)=H2O(g) △H= c kJ·mol-1
则反应2NO2(g)+4H2(g)=N2(g)+4H2O(1)的△H=_________。(用a、b、c表示)
(3)①合成氨反应的化学方程式为N2+3H2
 2NH3,该反应在固定容积的密闭容器中进行。下列各项标志着该反应达到化学平衡状态的是____________(填序号)
2NH3,该反应在固定容积的密闭容器中进行。下列各项标志着该反应达到化学平衡状态的是____________(填序号)A.容器内N2、H2、NH3的浓度之比为1∶3∶2
B.3v正(N2)=v逆(H2)
C.容器内压强保持不变
D.混合气体的相对分子质量保持不变
E.1mol N≡N键断裂,同时1mol H—H键断裂
②若在恒温条件下,将N2与H2按一定比例混合通入一个容积为2L的密闭容器中,5min反应达平衡,n(N2)=1mol,n(H2)=1mol,n(NH3)=2mol,则反应速率v(N2)=________________,H2的平衡转化率=_________________;若保持容器的温度不变,在10min时将容器的容积压缩为lL,请在答题卡坐标图中,画出从反应开始至15min时c(NH3)随时间变化曲线示意图。
汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化为无毒气体。
(1)汽车尾气中CO、NO2气体在一定条件下可以发生反应:
4CO(g)+2NO2(g) 4CO2(g)+N2(g) ΔH=-1200 kJ·mol-1
4CO2(g)+N2(g) ΔH=-1200 kJ·mol-1
①恒温恒容条件下,不能说明该反应已达到平衡状态的是________(填序号);
A.容器内混合气体颜色不再变化 B.容器内的压强保持不变
C.2v逆(NO2)=v正(N2) D.容器内混合气体密度保持不变
②能使该反应的反应速率增大,且平衡向逆反应方向移动的是________(填序号);
A.及时分离出CO2 B.适当升高温度
C.减小容器体积使体系压强增大 D.选择高效催化剂
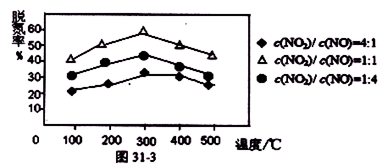
③对于该反应,温度不同(T2>T1)、其他条件相同时,下列图像正确的是________(填序号);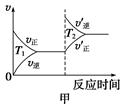
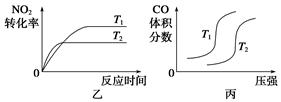
(2)汽车尾气中CO与H2O(g)在一定条件下可以发生反应:CO(g)+H2O(g) CO2(g)+H2(g) ΔH<0;820 ℃时在甲、乙、丙三个恒容密闭容器中,起始时按照右表进行投料,达到平衡状态时K=1.0。
CO2(g)+H2(g) ΔH<0;820 ℃时在甲、乙、丙三个恒容密闭容器中,起始时按照右表进行投料,达到平衡状态时K=1.0。
| 起始物质的量 | 甲 | 乙 | 丙 |
| n(H2O)/mol | 0.10 | 0.20 | 0.20 |
| n(CO)/mol | 0.10 | 0.10 | 0.20 |
①该反应的平衡常数表达式为___________;平衡时,甲容器中CO的转化率= ;
②平衡时,比较下列容器中CO的转化率:乙 甲(填“>”、“=”或“<”,下同);丙 甲。
25C时,用浓度为0.1000 mol/L的NaOH溶液滴定20. 00 mL 0 .1000 mol·L-1的
CH3COOH.。滴定曲线如图所示。下列分析错误的是
| A.C点的溶液:c(CH3COO一)+c(CH.3COOH)>c(Na+) |
| B.B点的溶液c (CH3COO一)>c(Na+)>c(H+)> c(OH-) |
| C.A点的纵坐标值为l |
| D.D点溶液2c(CH3COOH)十c(H+) =c(OH—)—c(CH3COO—) |
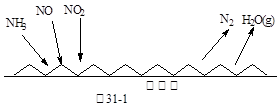
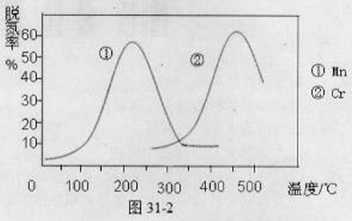
 H2SO3(l)
H2SO3(l)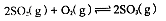 ,反应混合体系SO3的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态),根据图示回答下列问题:
,反应混合体系SO3的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态),根据图示回答下列问题: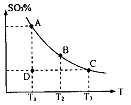
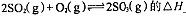 0(填“>”或“<”)。若在恒温恒容条件下,上述反应达到平衡,再给该平衡体系中通入SO3气体,容器内的压强 (填“增大”、“减小”或“不变”),平衡 移动(填“向正反应方何”、“逆反应方向’或“不”)若在恒温恒压条件下,上述反应达到平衡,再给该平衡体系中通人大量氮气后,体系重新达到平衡,此平衡与原平衡相比较,SO2的物质的量 __(填“增大”、“减小”或“不变”),O2的物质的量浓度 (填“增大”、“减小”或“不变”)。
0(填“>”或“<”)。若在恒温恒容条件下,上述反应达到平衡,再给该平衡体系中通入SO3气体,容器内的压强 (填“增大”、“减小”或“不变”),平衡 移动(填“向正反应方何”、“逆反应方向’或“不”)若在恒温恒压条件下,上述反应达到平衡,再给该平衡体系中通人大量氮气后,体系重新达到平衡,此平衡与原平衡相比较,SO2的物质的量 __(填“增大”、“减小”或“不变”),O2的物质的量浓度 (填“增大”、“减小”或“不变”)。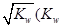 是水的离子积),则这两种溶液可为 (填字母)。
是水的离子积),则这两种溶液可为 (填字母)。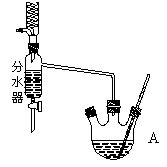

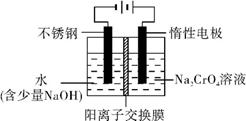
 8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2