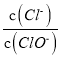题目内容
【题目】在恒容绝热(不与外界交换能量)条件下进行2A(g)+B(g)3C(g)+2D(s)反应,按下表数据投料,反应达到平衡状态,测得体系压强升高.
物质 | A | B | C | D |
起始投料/mol | 2 | 2 | 3 | 0 |
该反应的平衡常数表达式为K= . 升高温度,平衡常数将(填“增大”“减小”或“不变”).
【答案】![]() ;减小
;减小
【解析】解:在恒容绝热(不与外界交换能量)条件下进行2A(g)+B(g)3C(g)+2D(s)反应,其化学平衡常数K= ![]() ;反应前后气体的总物质的量不变,已知反应后体系压强升高,而气体的物质的量不变,说明温度升高,即该反应为放热反应,升高温度平衡向逆方向移动,则平衡常数减小;
;反应前后气体的总物质的量不变,已知反应后体系压强升高,而气体的物质的量不变,说明温度升高,即该反应为放热反应,升高温度平衡向逆方向移动,则平衡常数减小;
所以答案是: ![]() ;减小.
;减小.
【考点精析】解答此题的关键在于理解化学平衡状态本质及特征的相关知识,掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效).

练习册系列答案
 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目