题目内容
20. 请回答下列问题:
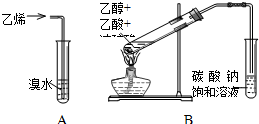
请回答下列问题:(1)图A溴水的颜色变化为红棕色褪色,试管中发生化学反应的方程式为:CH2=CH2+Br2→BrCH2CH2Br.
(2)图B是制取乙酸乙酯,该化学反应方程式为CH3COOH+CH3CH2OH?浓硫酸△CH3COOCH2CH3+H2O;
反应的试管中要加入几块碎玻璃或碎瓷片,其作用是防止暴沸,饱和碳酸钠溶液起的作用是降低乙酸乙酯的溶解度、吸收乙醇、除去挥发出来的乙酸.
分析 (1)乙烯含有碳碳双键,能使溴水褪色,此反应为加成反应;
(2)乙醇与乙酸在浓硫酸作催化剂条件下,加热生成乙酸乙酯和水,加热过程中为防止液体暴沸,需要加入沸石,实验室里用饱和碳酸钠溶液冷却乙酸乙酯的原因:除去乙酸和乙醇,并降低乙酸乙酯的溶解度,增大水的密度,使酯浮于水面,容易分层析出,便于分离.
解答 解:(1)乙烯通入溴水中,由于发生加成反应而使溴水褪色,发生的反应为:CH2=CH2+Br2→BrCH2CH2Br,故答案为:红棕色褪去;CH2=CH2+Br2→BrCH2CH2Br;
(2)乙醇与乙酸反应生成乙酸乙酯,条件下加热,浓硫酸作催化剂,方程式为:CH3COOH+CH3CH2OH?浓硫酸△CH3COOCH2CH3+H2O,加热过程中要加入少许碎瓷片以防止液体暴沸飞溅伤人,制备乙酸乙酯时常用饱和碳酸钠溶液吸收乙酸乙酯,主要是利用了乙酸乙酯难溶于饱和碳酸钠,乙醇与水混溶,乙酸能被碳酸钠吸收,易于除去杂质,故答案为:CH3COOH+CH3CH2OH?浓硫酸△CH3COOCH2CH3+H2O;防止暴沸;吸收乙醇、除去挥发出来的乙酸.
点评 本题主要考查的是乙烯的性质和乙酸乙酯的制取实验,涉及实验现象的描述和化学反应方程式的书写以及实验需要注意的事项,难度不大.

练习册系列答案
相关题目
11.分子式为C9H12O的有机物,有一个苯环、一个烃基,则它属于酚类的结构可能有( )
| A. | 2种 | B. | 4种 | C. | 5种 | D. | 6种 |
8.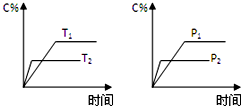 可逆反应aA(g)+bB(g)?cC(g)+dD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是( )
可逆反应aA(g)+bB(g)?cC(g)+dD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是( )
 可逆反应aA(g)+bB(g)?cC(g)+dD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是( )
可逆反应aA(g)+bB(g)?cC(g)+dD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是( )| A. | 化学方程式中a+b>c+d | |
| B. | 达平衡后,加入催化剂则C%增大 | |
| C. | 达平衡后,若升温,平衡逆向移动 | |
| D. | 其他条件不变,在不同温度达平衡后,C在T1时的反应速率大于T2 |
15.下列变化过程中,只破坏共价键的是( )
| A. | HCl溶于水得盐酸 | B. | NaCl颗粒被粉碎 | ||
| C. | I2升华 | D. | NH4Cl晶体加热分解 |
5.如图是氯气的制备以及氯、溴、碘的非金属性比较实验,充分反应一段时间后,打开装置D的活塞,将装置D中少量溶液加入装置E中,振荡,观察实验现象,下列说法正确的是( )
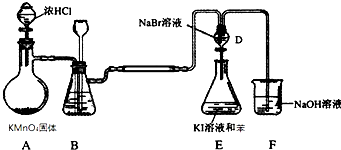

| A. | 装置E下层呈现紫红色 | |
| B. | 装置B中可盛放水吸收氯气中的HCl气体 | |
| C. | F2不能与NaCl溶液反应置换出氯气 | |
| D. | 装置E中有机试剂层呈现紫红色,能说明非金属性Br>I |
9.在强酸性或强碱性溶液中都能大量共存的一组离子是( )
| A. | Ba2+、Fe3+、Cl-、NO3- | B. | Na+、Ca2+、HCO3-、NO3- | ||
| C. | Al3+、NH4+、SO42-、Na+ | D. | Na+、K+、NO3-、SO42- |
10.下列电化学有关说法中正确的是( )
| A. | 将钢闸门与直流电源的正极相连,可降低钢闸门腐蚀速率 | |
| B. | 镀锌铁制品镀层受损后,铁制品仍不易生锈 | |
| C. | 粗铜精炼时,电镀液中的c(Cu2+)保持不变 | |
| D. | 纯银在空气中久置变黑发生的是电化学腐蚀 |
 .
.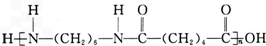 +(2n-1)H2O.
+(2n-1)H2O.