题目内容
15.下列变化过程中,只破坏共价键的是( )| A. | HCl溶于水得盐酸 | B. | NaCl颗粒被粉碎 | ||
| C. | I2升华 | D. | NH4Cl晶体加热分解 |
分析 物质形状的变化对化学键无影响,非金属与非金属之间以共价键结合,离子之间以离子键结合,电解质电离、化学变化中化学键均被破坏,以此来解答.
解答 解:A.HCl溶于水得盐酸,发生电离,H-Cl共价键断裂,故A选;
B.NaCl颗粒被粉碎,为形状的变化,化学键不变,故B不选;
C.I2升华,为形状的变化,化学键不变,故C不选;
D.NH4Cl晶体加热分解,离子键断裂,故D不选;
故选A.
点评 本题考查化学键,为高频考点,把握化学键的形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,注意铵盐中含离子键,题目难度不大.

练习册系列答案
相关题目
5.根据如图,判断下列说法中错误的是( )
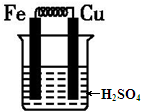

| A. | 铁电极为负极,铜电极为正极 | B. | 导线中电流方向为铁→铜 | ||
| C. | 溶液中阴离子移向铁电极 | D. | 正极电极反应式:2H++2e-═H2↑ |
6.下列有机物命名正确的是( )
| A. | 2-乙基丁烷 | B. | 2,2-二甲基-3-戊烯 | ||
| C. | 2,2-二甲基乙醇 | D. | 1,1,2,2-四溴乙烷 |
3.某种“自热米饭”,在食用时,将某液体加入到某白色固体中,放上装有冷米饭和蔬菜的盒子,过几分钟米饭就热气腾腾,非常方便.试推测该液体和固体最有可能的组合是( )
| A. | 硝酸铵和水 | B. | 浓硫酸和水 | C. | 生石灰和水 | D. | 苛性钠和水 |
10.下列说法正确的是( )
| A. | 甲烷的燃烧热为△H=-890.3kJ•mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | 已知H2O(l)═H2O(g)△H=+44 kJ•mol-1,则2gH2(g)完全燃烧生成液态水比生成气态水多释放22kJ的能量 | |
| C. | 吸热反应一定是非自发的化学反应 | |
| D. | 同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H相同 |
4.某铝热剂由铁红和铝组成.取a g该铝热剂样品,向其中加入足量的NaOH溶液,测得生成气体的体积为V1 L(标准状况,下同).
另取a g该样品将其引燃,恰好完全反应,待反应产物冷却后,加入足量稀盐酸,测得生成气体的体积为V2 L.若不考虑空气中O2的影响,则V1:V2为( )
另取a g该样品将其引燃,恰好完全反应,待反应产物冷却后,加入足量稀盐酸,测得生成气体的体积为V2 L.若不考虑空气中O2的影响,则V1:V2为( )
| A. | 3:2 | B. | 4:3 | C. | 1:1 | D. | 8:9 |
5.常温下,体积相同、pH也相同的HCl、HNO3、CH3COOH溶液分别与足量的NaHCO3溶液反应,产生CO2的体积( )
| A. | 同样多 | B. | HCl最多 | C. | HCl、HNO3一样多 | D. | CH3COOH最少 |
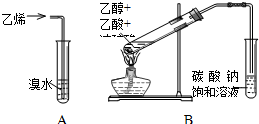 请回答下列问题:
请回答下列问题: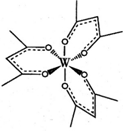 现有原子序数小于36的X、Y、Z、W四种元素.其中X元素的一种核素核内无中子;Y是地壳中含量最多的金属元素;Z原子的质量数为12,质子数与中子数相等;W的基态原子核外3d轨道上的电子数是最外层电子数的3倍.请回答下列问题:
现有原子序数小于36的X、Y、Z、W四种元素.其中X元素的一种核素核内无中子;Y是地壳中含量最多的金属元素;Z原子的质量数为12,质子数与中子数相等;W的基态原子核外3d轨道上的电子数是最外层电子数的3倍.请回答下列问题: