题目内容
如图所示,隔板K1固定不动,活塞K2可 自由移动。T℃时,M、
自由移动。T℃时,M、 N两个容器中均发生反应N2(g)+3H2(g)
N两个容器中均发生反应N2(g)+3H2(g) 2NH3(g),向容器M、N中各充入l mol N2和3 mol H2,初始M、N的容积和温度相同,并保持温度不变。下列有关说法中不正确的是 ( )
2NH3(g),向容器M、N中各充入l mol N2和3 mol H2,初始M、N的容积和温度相同,并保持温度不变。下列有关说法中不正确的是 ( )

 自由移动。T℃时,M、
自由移动。T℃时,M、 N两个容器中均发生反应N2(g)+3H2(g)
N两个容器中均发生反应N2(g)+3H2(g) 2NH3(g),向容器M、N中各充入l mol N2和3 mol H2,初始M、N的容积和温度相同,并保持温度不变。下列有关说法中不正确的是 ( )
2NH3(g),向容器M、N中各充入l mol N2和3 mol H2,初始M、N的容积和温度相同,并保持温度不变。下列有关说法中不正确的是 ( )
A.反应达到平衡时N2的转化率:M>N |
| B.H2的体积分数:M>N |
C.容器N中达到平衡,测得容器中含有1.2mol NH3,此时N的容积为VL,则该反应在此条件下的平衡常数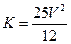 |
| D.该反应在T℃时的平衡常数K:M=N |
A
本题考查化学平衡与化学移动知识点。M为恒容容器,N为恒压容器,
N2(g)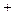 3H2(g)
3H2(g)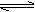 2NH3(g)是一个气体体积缩小的反应,随着反应的进行,N容器压强不变,M容器压强减小,N容器可以看成M容器加压,平衡正向移动,反应达到平衡时的转化率:M<N,H2体积分数M>N。平衡时N2、H2、NH3浓度分别为
2NH3(g)是一个气体体积缩小的反应,随着反应的进行,N容器压强不变,M容器压强减小,N容器可以看成M容器加压,平衡正向移动,反应达到平衡时的转化率:M<N,H2体积分数M>N。平衡时N2、H2、NH3浓度分别为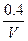
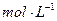 、
、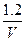
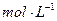 、
、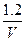
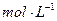 ,平衡常数
,平衡常数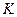 =
=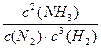
= =
=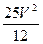 。平衡常数
。平衡常数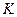 是温度的函
是温度的函 数,温度没变化,平衡常数
数,温度没变化,平衡常数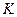 不变化。
不变化。
N2(g)
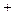 3H2(g)
3H2(g)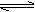 2NH3(g)是一个气体体积缩小的反应,随着反应的进行,N容器压强不变,M容器压强减小,N容器可以看成M容器加压,平衡正向移动,反应达到平衡时的转化率:M<N,H2体积分数M>N。平衡时N2、H2、NH3浓度分别为
2NH3(g)是一个气体体积缩小的反应,随着反应的进行,N容器压强不变,M容器压强减小,N容器可以看成M容器加压,平衡正向移动,反应达到平衡时的转化率:M<N,H2体积分数M>N。平衡时N2、H2、NH3浓度分别为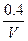
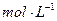 、
、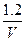
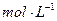 、
、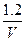
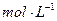 ,平衡常数
,平衡常数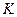 =
=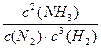
=
 =
=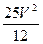 。平衡常数
。平衡常数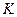 是温度的函
是温度的函 数,温度没变化,平衡常数
数,温度没变化,平衡常数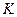 不变化。
不变化。
练习册系列答案
相关题目
 3Z(g)。下列说法不正确的是
3Z(g)。下列说法不正确的是 5 kJ/mol
5 kJ/mol  。(填序号)
。(填序号) c C(g)+d D(g) △H = -Q kJ/mol(Q为正值),达平衡状态后,下列结论中不正确的是
c C(g)+d D(g) △H = -Q kJ/mol(Q为正值),达平衡状态后,下列结论中不正确的是 C(g)+ 2D(g),2分钟末反应达到平衡状态,D的浓度为0.4 mol·L-1,求
C(g)+ 2D(g),2分钟末反应达到平衡状态,D的浓度为0.4 mol·L-1,求 H2+CO2若起始浓度[CO]为2mol/L、[H2O]=
H2+CO2若起始浓度[CO]为2mol/L、[H2O]= 3mol/L,反应达到平衡时,CO的转化率为60%;如果将H2O的起始浓度加大到6mol/L,则CO的转化率为75%。请注意上述有关数据,并总结出规律,完成下列问题:
3mol/L,反应达到平衡时,CO的转化率为60%;如果将H2O的起始浓度加大到6mol/L,则CO的转化率为75%。请注意上述有关数据,并总结出规律,完成下列问题: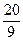 时,b=
时,b= 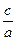 =
=  2NH3(g);△H=" " -92.2KJ·mol-1,已知:平衡时容器内气体的压强为开始的80%.
2NH3(g);△H=" " -92.2KJ·mol-1,已知:平衡时容器内气体的压强为开始的80%. 到平衡状态时,放出的热量为
到平衡状态时,放出的热量为  __
__