题目内容
【题目】已知二元酸H2A的电离方程式为:H2A=H++HA-,HA-![]() H++A2-,下列有关该酸及盐的说法正确的是
H++A2-,下列有关该酸及盐的说法正确的是
A.0.1 mol/LH2A溶液pH=1
B.H2A为强酸
C.NaHA溶液呈酸性的原因是:HA-+H2O![]() H2A+OH-
H2A+OH-
D.Na2A在溶液中不水解,溶液呈中性
【答案】B
【解析】
A. 根据电离方程式可知:H2A第一步完全电离,第二步存在电离平衡电离产生H+,所以0.1 mol/LH2A溶液中c(H+)大于0.1 mol/L,故该溶液pH<1,A错误;
B. H2A第一步完全电离,因此H2A为强酸,B正确;
C. NaHA溶液呈酸性的原因是:HA-会发生电离作用,产生H+,电离方程式为:HA-![]() H++A2-,C错误;
H++A2-,C错误;
D. Na2A是强碱弱酸盐,在溶液A2-发生水解作用,消耗水电离产生的H+,使溶液呈碱性,D错误;
故合理选项是B。

【题目】毒重石的主要成分为BaCO3(含Ca2+、Mg2+、Fe3+等杂质)。实验室利用毒重石制备BaCl2·2H2O的流程如图:
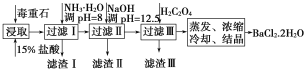
(1)毒重石用盐酸浸取前需充分研磨,目的是__。
(2)加入NH3·H2O调pH=8可除去__(填离子符号),滤渣Ⅱ中含__(填化学式)。加入H2C2O4时应避免过量,原因是__。
已知:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9
Ca2+ | Mg2+ | Fe3+ | |
开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
完全沉淀时的pH | 13.9 | 11.1 | 3.2 |
(3)利用间接酸碱滴定法可测定Ba2+的含量,实验分两步进行。
已知:2CrO42-+2H+=Cr2O72-+H2O
Ba2++CrO42-=BaCrO4↓
步骤Ⅰ:移取xmL一定浓度的Na2CrO4溶液于锥形瓶中,加入酸碱指示剂,用bmol·L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V0mL。
步骤Ⅱ:移取ymLBaCl2溶液于锥形瓶中,加入xmL与步骤Ⅰ相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用bmol·L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1mL。
滴加盐酸标准液时应使用酸式滴定管,“0”刻度位于滴定管的__(填“上方”或“下方”)。BaCl2溶液的浓度为__mol·L-1。若步骤Ⅱ中滴加盐酸时有少量待测液溅出,Ba2+浓度测量值将__(填“偏大”或“偏小”)。