题目内容
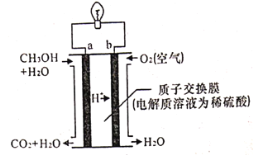
【题目】美国斯坦福大学的工程师设计出一种从污水“提取”潜在电能的新型微生物电池,该电池能将生活污水中的有机物分解同时发电,电池结构如图所示。已知a电极为惰性材料,b电极为Ag2O。下列说法不正确的是( )
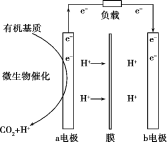
A.a电极是负极,b电极是正极
B.b电极发生的反应是Ag2O+2e-+2H+=2Ag+H2O
C.a电极每生成标准状况下2.24LCO2,可向b电极转移0.1mol电子
D.高温条件下,该电池不能正常工作
【答案】C
【解析】
A选项,根据题图中电子流动方向,可判断a电极是负极,b电极是正极,故A正确;
B选项,b电极是正极,Ag2O得到电子发生还原反应,电极反应式为Ag2O+2e-+2H+=2Ag+H2O,故B正确;
C选项,a电极发生反应的有机基质是什么物质未说明,故电子转移的数目无法确定,故C错误;
D选项,高温条件下,微生物会死亡,导致电池无法正常工作,故D正确。
综上所述,答案为C。

 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案【题目】丙烯酸甲酯(CH2=CHCOOCH3)是一种重要的有机化工原料。实验室制备少量丙烯酸甲酯的反应为:CH2=CHCOOH+CH3OH![]() CH2=CHCOOCH3+H2O,步骤如下:
CH2=CHCOOCH3+H2O,步骤如下:
步骤1:在100mL圆底烧瓶中依次加入10.0g丙烯酸、少许碎瓷片、10mL甲醇和2mL浓硫酸,搅拌。
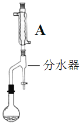
步骤2:如图,连接装置,加热烧瓶中的混合液,用锥形瓶盛接通过分水器分离出的水。当不再有水生成,停止加热。
步骤3:反应液冷却后,依次用5%Na2CO3溶液、饱和食盐水、水洗涤。分离出有机相。
步骤4;向有机相中加无水Na2SO4固体,过滤后蒸馏,收集70~90℃馏分。测得丙烯酸甲酯的质量为6.45g。
可能用到的信息:
密度 | 沸点 | 溶解性 | ||
丙烯酸 | 1.05g·cm-3 | 141℃ | 与水互溶,易溶于有机溶剂 | 有毒 |
甲醇 | 0.79g·cm-3 | 65℃ | 与水互溶,易溶于有机溶剂 | 易挥发,有毒 |
丙烯酸甲酯 | 0.95g·cm-3 | 80.5℃ | 难溶于水,易溶于有机溶剂 | 易挥发 |
请回答下列问题:
(1)步骤1中,加入碎瓷片的目的是__。
(2)步骤2中,图中所示装置中仪器A的名称是__,其作用为__。
(3)步骤3中,用5%Na2CO3溶液洗涤后,分离有机相的操作名称为__。
(4)实验中可能生成的有机副产物结构简式为__(填一种即可)。
(5)本实验中丙烯酸甲酯的产率为__%。
【题目】某班同学用以下实验探究![]() 、
、![]() 的性质。回答下列问题:
的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁、溴化亚铁固体,均配制成![]() 的溶液。在
的溶液。在![]() 溶液中需加入少量铁屑,其目的是_____________________________________。
溶液中需加入少量铁屑,其目的是_____________________________________。
(2)甲组同学取![]() 溶液,加入几滴氯水,再加入1滴
溶液,加入几滴氯水,再加入1滴![]() 溶液,溶液变红,说明
溶液,溶液变红,说明![]() 可将
可将![]() 氧化。
氧化。![]() 溶液与氯水反应的离子方程式为____________________。
溶液与氯水反应的离子方程式为____________________。
(3)乙组同学认为甲组的实验不够严谨,该组同学在![]() 溶液中先加入
溶液中先加入![]() 煤油,再向下层溶液中依次加入几滴氯水和1滴
煤油,再向下层溶液中依次加入几滴氯水和1滴![]() 溶液,溶液变红。煤油的作用是_________________________。
溶液,溶液变红。煤油的作用是_________________________。
(4)丙组同学取![]() 上述
上述![]() 溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
假设1:![]() 被
被![]() 氧化成
氧化成![]() 溶解在溶液中;
溶解在溶液中;
假设2:![]() 被
被![]() 氧化成
氧化成![]() 。
。
请你完成下表,验证假设
实验步骤、预期现象 | 结论 |
①向溶液中加入____________,振荡、静置现象:____________ | 假设1正确 |
②向溶液中加入____________,现象:____________ | 假设2正确 |
(5)已知:![]() 。若在
。若在![]() 上述
上述![]() 溶液中通入标准状况
溶液中通入标准状况![]() ,反应的离子方程式为________________________________。
,反应的离子方程式为________________________________。