题目内容
【题目】用中和滴定法测定烧碱的纯度,若烧碱中含有少量不与酸作用的可溶性杂质,试根据实验回答:
(1)准确称取4.0g烧碱样品。
(2)将样品配成250mL待测液。
(3)用____________(填仪器名称)量取25.00mL待测液于锥形瓶中,并滴加几滴甲基橙作指示剂。
(4)用0.2010 mol·L-1标准盐酸滴定待测烧碱溶液,滴定时,两眼注视____________,直到滴定终点。达到终点的具体现象是:____________。
(5)若两次实验滴定的数据如下表:
滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
滴定前读数(mL) | 滴定后读数(mL) | ||
第一次 | 25.00 | 0.50 | 20.40 |
第二次 | 25.00 | 5.00 | 28.30 |
第三次 | 25.00 | 4.00 | 24.10 |
根据上述各数据,计算烧碱的纯度:____________
(6)下列操作中,会导致所测得的烧碱的纯度偏大的是________。
a.滴定终点时,俯视刻度
b.没有用盐酸标准溶液润洗相应的滴定管
c.锥形瓶中有少量的蒸馏水
【答案】碱式滴定管 锥形瓶中溶液颜色变化 滴入最后一滴标准液,溶液由黄色变为橙色,且半分钟不变回原色。 40.2% b
【解析】
(3)用碱式滴定管量取烧碱溶液于锥形瓶中
(4)根据滴定规范性的操作要求答题;
(5)根据数据的有效性计算消耗的盐酸标准液的平均体积,再结合公式c(测) =  计算,进而计算纯度;
计算,进而计算纯度;
(6)根据错误操作对消耗的标准盐酸溶液体积的影响来分析作答。
(3)烧碱属于碱,在中和滴定中需用碱式滴定管量取,用锥形瓶盛放待测液,故答案为:碱式滴定管;
(4)滴定时左手旋转酸式滴定管,右手不停地摇动锥形瓶,两眼需注视锥形瓶中溶液颜色变化;滴定终点现象是:滴入最后一滴标准液,溶液由黄色变为橙色,且半分钟不变回原色,故答案为:锥形瓶中溶液颜色变化;滴入最后一滴标准液,溶液由黄色变为橙色,且半分钟不变回原色;
(5)由表格信息可知,标准液的体积分别为:(20.40-0.50) mL =19.90mL,(28.30-5.00)mL=23.30mL,(24.10-4.00)=20.10mL,则可知第二组数据误差较大,无效,消耗的盐酸溶液平均体积为![]() =20.00mL,代入公式c(测) =
=20.00mL,代入公式c(测) =  可得:=
可得:=![]() =0.1608molL1,则250mL待测液中氢氧化钠的物质的量为0.1608molL1
=0.1608molL1,则250mL待测液中氢氧化钠的物质的量为0.1608molL1![]() 0.25L=0.0402 mol,烧碱的纯度=
0.25L=0.0402 mol,烧碱的纯度=![]() =40.2%,故答案为:40.2%;
=40.2%,故答案为:40.2%;
(6) a.滴定终点时,俯视刻度,则读数偏小,所有标准溶液的体积偏小,求出的待测液的浓度偏小,最终导致纯度偏小,不符合题意,a不选;
b.没有用盐酸标准溶液润洗相应的滴定管,则标准液被稀释,消耗的标准液的体积偏大,使待测液的浓度计算偏大,最终导致纯度偏大,符合题意,b项选;
c.锥形瓶中有少量的蒸馏水,对所测待测液的浓度无影响,不符合题意,c项不选;
故答案为:b。

 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
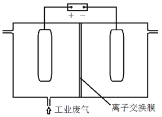
名校名卷单元同步训练测试题系列答案【题目】高铁酸钠(Na2FeO4)是具有紫色光泽的粉末,是一种高效绿色强氧化剂,碱性条件下稳定,可用于废水和生活用水的处理。实验室以石墨和铁钉为电极,以不同浓度的NaOH溶液为电解质溶液,控制一定电压电解制备高铁酸钠,电解装置和现象如下:
c(NaOH) | 阴极现象 | 阳极现象 |
1 mol·L-1 | 产生无色气体 | 产生无色气体,10min内溶液颜色无明显变化 |
10 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,3min后溶液变为浅紫红色,随后逐渐加深 |
15 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,1min后溶液变为浅紫红色,随后逐渐加深 |
下列说法不正确的是

A. a为铁钉,b为石墨
B. 阴极主要发生反应:2H2O + 2e-=== H2↑+ 2OH-
C. 高浓度的NaOH溶液,有利于发生Fe-6e-+ 8OH-=== FeO42-+ 4H2O
D. 制备Na2FeO4时,若用饱和NaCl溶液,可有效避免阳极产生气体