题目内容
【题目】下列事实不能用勒夏特列原理解释的是( )
A.对于2HI(g)![]() H2(g)+ I2(g),达平衡后,缩小容器体积可使体系颜色变深
H2(g)+ I2(g),达平衡后,缩小容器体积可使体系颜色变深
B.合成氨反应中为提高氨的产率,理论上应采取降低温度的措施
C.实验室配制FeCl3溶液时,将FeCl3固体加入到少量的浓盐酸中再加水稀释
D.用饱和食盐水可以去除Cl2中的HCl
【答案】A
【解析】
A.2HI(g)![]() H2(g)+ I2(g),反应前后气体分子数不变,缩小体积,压强变大,平衡不移动,不能用勒夏特列原理解释,A符合;
H2(g)+ I2(g),反应前后气体分子数不变,缩小体积,压强变大,平衡不移动,不能用勒夏特列原理解释,A符合;
B.合成氨的反应为放热反应,温度降低,平衡正向移动,氨的产率提高,能用勒夏特列原理解释,B不符合;
C.配制FeCl3溶液,在少量浓盐酸中加水稀释,抑制铁离子的水解,能用勒夏特列原理解释,C不符合;
D.Cl2+H2O![]() HCl+HClO,饱和食盐水中氯离子的浓度很高,根据勒夏特列原理,氯离子的浓度高能使该反应平衡逆向移动,抑制该反应进行的程度,能减小氯气在水中的溶解,能用勒夏特列原理解释,D不符合;故答案为:A。
HCl+HClO,饱和食盐水中氯离子的浓度很高,根据勒夏特列原理,氯离子的浓度高能使该反应平衡逆向移动,抑制该反应进行的程度,能减小氯气在水中的溶解,能用勒夏特列原理解释,D不符合;故答案为:A。

 特高级教师点拨系列答案
特高级教师点拨系列答案【题目】化学是一门以实验为基础的科学。
(1)用下列实验装置完成对应的实验(部分仪器略去),能达到实验目的的是________(填字母)。
A | B | C | D |
|
|
|
|
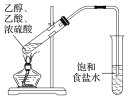
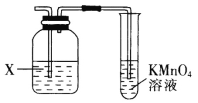
干燥氯气 | 吸收NH3 | 石油的分馏 | 制取乙酸乙酯 |
(2)为除去粗盐中的MgCl2、CaCl2、Na2SO4以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
![]()
①第Ⅰ步操作的名称是____________。
②若第Ⅱ、Ⅳ步顺序颠倒,是否会对实验结果产生影响?________(填“有影响”或“无影响”)。
③第Ⅴ步操作所需玻璃仪器的名称是____________。
【题目】碱式氧化(NiOOH)可用废镍催化剂(主要含Ni、Al,少量Cr、FeS等)来制备,其工艺流程如下:
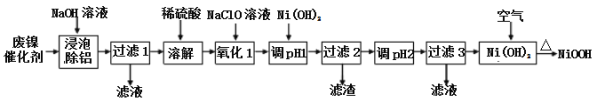
回答下列问题:
(1)“浸泡除铝”时,发生反应的离子反应方程式为_____________________。
(2)“过滤1”用到的玻璃仪器________________________________________。
(3)已知该条件下金属离子开始沉淀和完全沉淀的pH如下表:
开始沉淀的pH | 完全沉淀的pH | |
Ni2+ | 6.2 | 8.6 |
Fe2+ | 7.6 | 9.1 |
Fe3+ | 2.3 | 3.3 |
Cr3+ | 4.5 | 5.6 |
“调pH 1”时,溶液pH范围为_______________;
(4)在空气中加热Ni(OH)2可得NiOOH,请写出此反应的化学方程式________________。
(5)在酸性溶液中CrO![]() 可以转化成Cr2O
可以转化成Cr2O![]() ,用离子方程式表示该转化反应__________,已知BaCrO4的Ksp=1.2×10-10,要使溶液中CrO
,用离子方程式表示该转化反应__________,已知BaCrO4的Ksp=1.2×10-10,要使溶液中CrO![]() 沉淀完全(c(CrO
沉淀完全(c(CrO![]() )≦1×10-5mol·L1),溶液中钡离子浓度至少为________mol·L1。
)≦1×10-5mol·L1),溶液中钡离子浓度至少为________mol·L1。