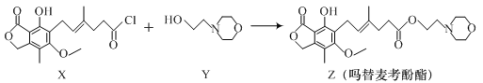
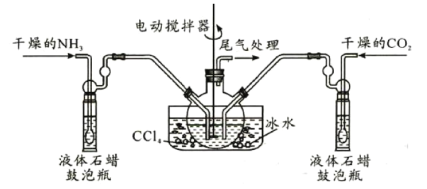
题目内容
【题目】I、有一种金属单质A,焰色反应呈黄色,能发生下图所示的变化:
![]()
上图中淡黄色固体B是__________;其与H2O反应的化学方程式为__________________。写出上图中的C溶液与硝酸溶液反应的化学方程式_____________________。
II、下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素。 请根据要求回答问题:

(1)②的元素符号是__________;该元素的最高价氧化物的电子式为__________;
(2)⑤和⑥两种元素的非金属性强弱关系是:⑤________⑥(填“>”或“<”);
(3)①和③两种元素组成的化合物中含有的化学键为__________(填“离子键”或“共价键”)
(4)④和⑥两种元素组成的化合物与AgNO3溶液反应的离子方程式为______________。
【答案】Na2O2 2Na2O2+2H2O=4NaOH+O2↑ HNO3+NaOH=NaNO3+H2O C ![]() < 共价键 Cl-+Ag+=AgCl↓
< 共价键 Cl-+Ag+=AgCl↓
【解析】
I.根据转化关系及现象可判断,A是Na,B是Na2O2,C是氢氧化钠。其中过氧化钠与水反应的方程式2Na2O2+2H2O=4NaOH+O2↑;NaOH溶液与HNO3溶液反应的化学方程式为:HNO3+NaOH=NaNO3+H2O,故答案为:Na2O2;2Na2O2+2H2O=4NaOH+O2↑;HNO3+NaOH=NaNO3+H2O;
II.由元素在周期表的位置可知,①~⑥分别为H、C、O、Na、S、Cl。
(1)②的元素符号是C,其最高价氧化物为二氧化碳,二氧化碳分子中碳原子与氧原子之间形成2对共用电子对,电子式为![]() ,故答案为:C;
,故答案为:C;![]() ;
;
(2)同周期元素的原子序数越大,非金属性越强,则非金属性为⑤<⑥,故答案为:<;
(3)①和③两种元素组成的化合物为水和双氧水,二者都属于共价化合物,只含有共价键,故答案为:共价键;
(4)④和⑥两种元素组成的化合物为NaCl,NaCl与AgNO3溶液反应的离子反应为:Cl-+Ag+=AgCl↓,故答案为:Cl-+Ag+=AgCl↓。