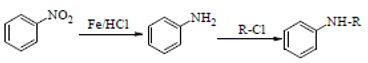
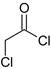
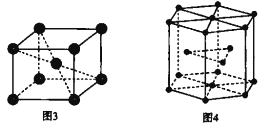
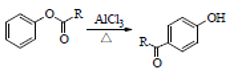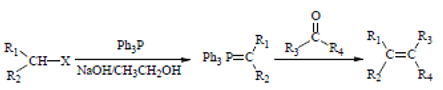题目内容
【题目】铝粉可以除去废液中的NaNO3,发生反应的化学方程式为:10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O,回答下列问题:
(1)该反应的离子方程式为_____________________________。
(2)该反应的还原剂为___________(填化学式,下同),还原产物为_____________。
(3)2.7g铝粉参与反应,溶液的质量增加_________g。
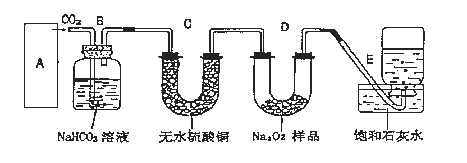
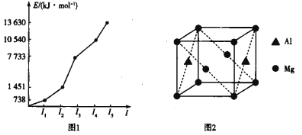
(4)铝箔表面易形成致密的氧化膜,加热铝箔,铝箔熔化但不滴落,说明____________。
【答案】10Al+6NO3-+4OH-=10AlO2-+3N2↑+2H2O Al N2 1.86 Al2O3熔点高
【解析】
(1)NaNO3、NaOH、NaAlO2都是易溶于水的强电解质,书写离子方程式时,将它们改写为离子,然后删去两边未参加反应的离子。
(2)该反应的还原剂为含化合价升高元素的反应物,还原产物为含化合价降低元素的生成物。
(3)2.7g铝粉参与反应,溶液的质量增加应为铝的质量与NO质量之差。
(4)铝箔表面易形成致密的氧化膜,加热铝箔,铝箔熔化但不滴落,说明铝的熔化温度比氧化铝的熔化温度低。
(1)将化学方程式10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O中的NaNO3、NaOH、NaAlO2改写为离子,即得10Al+6Na++6NO3-+4Na++4OH-=10Na++10AlO2-+3N2↑+2H2O,然后删去两边未参加反应的Na+,即得离子方程式为10Al+6NO3-+4OH-=10AlO2-+3N2↑+2H2O。答案为:10Al+6NO3-+4OH-=10AlO2-+3N2↑+2H2O;
(2)10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O中,还原剂为Al,还原产物为N2。答案为:Al;N2;
(3)设溶液的质量增加为x
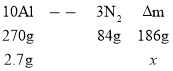
由观察可得出,x=1.86g。答案为:1.86。
(4)铝箔表面易形成致密的氧化膜,加热铝箔,铝箔熔化但不滴落,说明铝的熔化温度比氧化铝的熔化温度低。答案为:Al2O3熔点高。

 名师指导期末冲刺卷系列答案
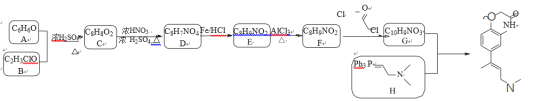
名师指导期末冲刺卷系列答案【题目】腈亚胺与邻酚羟基苄醇在碱的作用下可以发生偶联反应生成醚键,反应的条件温和,操作简单,目标产物收率高。下面是利用该方法合成化合物H的一种方法:
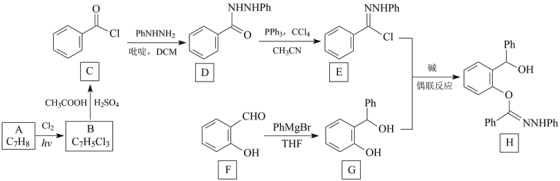
注:以上合成路线中,Ph代表苯基,如PhNHNH2表示![]() 。
。
实验 | 碱 | 温度/℃ | 溶剂 | 产率% |
1 | Et3N | 25 | DCM | <10 |
2 | 吡啶 | 25 | DCM | <5 |
3 | Cs2CO3 | 25 | DCM | 70 |
4 | LiOtBu | 25 | DCM | 43 |
5 | Cs2CO3 | 25 | DMF | 79 |
6 | Cs2CO3 | 25 | CH3CN | 83 |
回答下列问题:
(1)A的化学名称为_________,B的结构简式为___________。
(2)由C生成D的反应类型是________,F中的官能团名称是___________。
(3)H的分子式为_______________。
(4)不同条件对偶联反应生成H产率的影响如上表:
观察上表可知,当选用DCM作溶剂时,最适宜的碱是____________,由实验3、实验4和实验5可得出的结论是:25℃时,____________________,H产率最高。
(5)X为G的同分异构体,写出满足下列条件的X的结构简式:____________。
①所含苯环个数与G相同;②有四种不同化学环境的氢,其个数比为1:1:2:2
(6)利用偶联反应,以![]() 和化合物D为原料制备
和化合物D为原料制备 ,
,
写出合成路线:____________________________。(其他试剂任选)