题目内容
【题目】下列实验设计正确的是( )
操作 | 现象 | 结论 | |
A | 将SO2通入溴水 | 溴水褪色 | SO2具有漂白性 |
B | 将乙烯通入酸性KMnO4溶液 | 酸性KMnO4溶液褪色 | 乙烯具有还原性 |
C | 将澄清石灰水滴入某溶液 | 出现白色浑浊 | 其溶液中存在CO32- |
D | 将硝酸银溶液滴入某溶液 | 出现白色沉淀 | 其溶液中存在Cl- |
A.AB.BC.CD.D
【答案】B
【解析】
本题主要考查物质性质与实验设计。
A.SO2与溴水发生氧化还原反应:![]() ,SO2中S元素化合价升高,被氧化,体现了SO2的还原性,故A错误。
,SO2中S元素化合价升高,被氧化,体现了SO2的还原性,故A错误。
B.乙烯能被酸性高锰酸钾溶液氧化,使酸性高锰酸钾溶液褪色,体现了乙烯的还原性,故B正确。
C.与澄清石灰水反应使石灰水变浑浊的不一定是![]() ,也有可能是
,也有可能是![]() 、
、![]() 、
、![]() ,故C错误。
,故C错误。
D.与硝酸银反应生成白色沉淀的不一定是Cl-,也有可能是![]() 等,故D错误。
等,故D错误。
答案选B。

 快捷英语周周练系列答案
快捷英语周周练系列答案【题目】软锰矿的主要成分是MnO2,还含有少量金属铁、镁、铝、锌、铜的化合物等杂质。黄铁矿的主要成分是FeS2,还含有硅、铝的氧化物等杂质。工业上用软锰矿制备碳酸锰并回收硫酸铵,其主要流程如下:
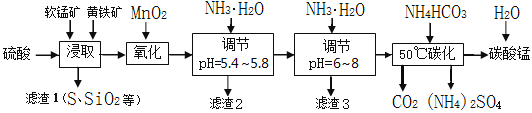
已知金属离子从开始形成氢氧化物沉淀,到沉淀时溶液的pH如下表:
金属离子 | Fe2+ | Fe3+ | Al3+ | Cu2+ | Mn2+ |
开始沉淀pH | 7.5 | 2.7 | 4.1 | 5.9 | 8.8 |
完全沉淀pH | 9.5 | 3.7 | 5.4 | 6.9 | 10.8 |
(1)提高浸出率的可采取的措施有_________。
A.适当升高温度 B.搅拌 C.加适量纯碱 D.加压
(2)浸取完成后,取浸取液少许,加入KSCN溶液无明显现象,则浸取时发生的主要反应的化学方程式是____________________________________________。
(3)调节pH为5.4~5.8的目的是_____________________________________________。
(4)滤渣3的主要成分的化学式是_____________。
(5)50℃碳化过程发生反应的离子方程式是____________________________________。