题目内容
【题目】A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去)。
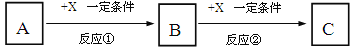
(1)若X是空气中存在的强氧化性无色气体单质,则A可能是___________(填序号)
a.C b.N2 c.S d.Al
(2)若X是日常生活中最常用的金属单质,A是气体单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,X在气体A中燃烧产生棕黄色的烟。
B的化学式为____________; 反应②的化学方程式为:___________________,
C溶液中加入NaOH溶液后产生的现象是_________________________, 方程式为____________________________________、_________________________________。
【答案】a b cFeCl32 FeCl3 + Fe = 3 FeCl2先生成白色沉淀,很快变成灰绿,最终变成红褐色FeCl2+2NaOH=Fe(OH)2↓+2NaCl4Fe(OH)2 +O2+2H2O=4Fe(OH)3
【解析】
(1)依据转化关系,若X是空气中存在的强氧化性无色气体单质为O2,AB中含有被氧化的元素,化合价升高,所以A所含元素有变价;
a.转化关系为:C![]() CO
CO![]() CO2,故a符合;b.N2
CO2,故a符合;b.N2![]() NO
NO![]() NO2,故b符合;c.转化关系为:S
NO2,故b符合;c.转化关系为:S![]() SO2
SO2![]() SO3,故c符合;d、Mg无变价,不能实现转化关系,故d不符合;故答案为abc;
SO3,故c符合;d、Mg无变价,不能实现转化关系,故d不符合;故答案为abc;
(2)若X是日常生活中最常用的金属单质,A是气体单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀说明溶液中含氯离子,证明A为Cl2,X在气体A中燃烧产生棕黄色的烟,X为Fe,转化关系为:Cl2![]() FeCl3
FeCl3![]() FeCl2,可知B为FeCl3,反应②的化学方程式为2 FeCl3 + Fe =3FeCl2; C(Fe2+)溶液中加入NaOH溶液后产生的现象是生成白色氢氧化亚铁沉淀,迅速变成灰绿色,最后变为红褐色,涉及反应方程式为FeCl2+2NaOH=Fe(OH)2↓+2NaCl,4Fe(OH)2 +O2+2H2O=4Fe(OH)3;
FeCl2,可知B为FeCl3,反应②的化学方程式为2 FeCl3 + Fe =3FeCl2; C(Fe2+)溶液中加入NaOH溶液后产生的现象是生成白色氢氧化亚铁沉淀,迅速变成灰绿色,最后变为红褐色,涉及反应方程式为FeCl2+2NaOH=Fe(OH)2↓+2NaCl,4Fe(OH)2 +O2+2H2O=4Fe(OH)3;

【题目】某化学研究性学习小组对某Na2CO3和NaHCO3的混合溶液的组成进行探究,取20.0mL该混合溶液,向其中不断加入1.00mol·L﹣1的稀盐酸,加入稀盐酸的体积和产生的现象如表中所示.
反应阶段 | Ⅰ | Ⅱ | Ⅲ |
稀盐酸体积x/mL | 0<x≤10.0 | 10.0<x≤40.0 | x>40.0 |
现 象 | 无气体 | 有气体 | 无气体 |
则混合溶液中c(HCO3﹣)为( )
A. 1.00mol·L﹣1 B. 0.50mol·L﹣1 C. 1.50mol·L﹣1 D. 2.00mol·L﹣1