题目内容
下列实验现象所对应的离子方程式不正确的是( )
| A、向NaAlO2溶液中通入过量CO2:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3 |
| B、向Ba(OH)2溶液中加入稀H2SO4恰好完全反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
| C、向稀NaOH溶液氯水中加入:Cl2+2OH-═Cl-+ClO-+H2O |
| D、向FeCl2溶液中加入少量K3[Fe(CN)3]溶液:3Fe2++2[Fe(CN)3]3-═Fe3[Fe(CN)2]2↓ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.二氧化碳过量,偏铝酸钠溶液与二氧化碳反应生成氢氧化铝沉淀和碳酸氢钠;
B.氢离子和氢氧根离子的化学计量数错误,不满足氢氧化钡和硫酸的化学式组成;
C.氢氧化钠溶液与氯气反应生成氯化钠、次氯酸钠和水;
D.此反应为检验亚铁离子的方法,亚铁离子能够与[Fe(CN)3]3-离子反应生成Fe3[Fe(CN)2]2沉淀.
B.氢离子和氢氧根离子的化学计量数错误,不满足氢氧化钡和硫酸的化学式组成;
C.氢氧化钠溶液与氯气反应生成氯化钠、次氯酸钠和水;
D.此反应为检验亚铁离子的方法,亚铁离子能够与[Fe(CN)3]3-离子反应生成Fe3[Fe(CN)2]2沉淀.
解答:
解:A.NaAlO2溶液中通入过量CO2,反应生成碳酸氢根离子,反应的离子方程式为:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3,故A正确;
B.Ba(OH)2溶液中加入稀H2SO4恰好完全反应,氢离子和氢氧根离子的计量数为2,正确的离子方程式为:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O,故B错误;
C.稀NaOH溶液加入氯水,反应生成氯化钠、次氯酸钠和水,反应的离子方程式为:Cl2+2OH-═Cl-+ClO-+H2O,故C正确;
D.FeCl2溶液中加入少量K3[Fe(CN)3]溶液,反应生成Fe3[Fe(CN)2]2沉淀,反应的离子方程式为:3Fe2++2[Fe(CN)3]3-═Fe3[Fe(CN)2]2↓,故D正确;
故选B.
B.Ba(OH)2溶液中加入稀H2SO4恰好完全反应,氢离子和氢氧根离子的计量数为2,正确的离子方程式为:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O,故B错误;
C.稀NaOH溶液加入氯水,反应生成氯化钠、次氯酸钠和水,反应的离子方程式为:Cl2+2OH-═Cl-+ClO-+H2O,故C正确;
D.FeCl2溶液中加入少量K3[Fe(CN)3]溶液,反应生成Fe3[Fe(CN)2]2沉淀,反应的离子方程式为:3Fe2++2[Fe(CN)3]3-═Fe3[Fe(CN)2]2↓,故D正确;
故选B.
点评:本题考查了离子方程式的正误判断,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式等,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
相关题目
某合作学习小组讨论辨析以下说法正确的是( )
①粗盐和酸雨都是混合物
②硅是光导纤维的主要成分,SiO2可用于太阳能电池
③向某溶液中滴加KSCN 溶液,溶液不变色,滴加氯水后溶液显红色,该溶液中一定含Fe2+
④不锈钢和目前流通的硬币都是合金
⑤氢气在氧气或氯气中燃烧,都能观察到淡蓝色火焰
⑥纯碱和熟石灰都是碱.
①粗盐和酸雨都是混合物
②硅是光导纤维的主要成分,SiO2可用于太阳能电池
③向某溶液中滴加KSCN 溶液,溶液不变色,滴加氯水后溶液显红色,该溶液中一定含Fe2+
④不锈钢和目前流通的硬币都是合金
⑤氢气在氧气或氯气中燃烧,都能观察到淡蓝色火焰
⑥纯碱和熟石灰都是碱.
| A、①③④ | B、①②③④⑥ |
| C、③④⑤⑥ | D、①②④⑤ |
常温下,Na2CO3溶液中存在平衡:CO32-+H2O?HCO3-+OH-,下列有关该溶液的说法正确的是( )
| A、离子浓度:c(Na+)>c(CO32-)>c(OH-)>c(H+) |
| B、升高温度,平衡向右移动 |
| C、滴入CaCl2浓溶液,溶液的pH增大 |
| D、加入NaOH固体,溶液的pH减小 |
碳化铁(Fe3C)在冶金上称为渗碳体,为灰白色结晶粉末,与一定浓度的HNO3反应,生成Fe(NO3)3、NO2、NO、CO2和水.当产物中n(NO2):n(NO)=1:1时,下列说法正确的是( )
| A、反应中生成标况下2.24L CO2时转移电子数目为1.3NA |
| B、参加反应的Fe3C和HNO3的物质的量之比为1:9 |
| C、反应中产生CO2和NO2的体积比为1:4 |
| D、此反应中氧化剂是HNO3,氧化产物是NO2和NO |
下列说法中,正确的是( )
| A、铝箔在酒精灯火焰上加热熔化但不滴落,说明铝箔表面氧化铝膜的熔点高于铝 |
| B、向氢氧化铁胶体中加入少量稀硫酸,因发生化学反应而产生红褐色沉淀 |
| C、电子工业用30%的氯化铁溶液腐蚀敷在印刷线路板上的铜箔:Fe3++Cu═Fe2++Cu2+ |
| D、标况下,NA个SO2分子和NA个SO3分子的体积相同(NA表示阿伏加德罗常数值) |
某小组为研究电化学原理,设计如图装置.下列叙述不正确的是( )


| A、a和b分别与电源的负极、正极相连时,电解氯化钠溶液产生氯气 |
| B、a和b用导线连接时,碳棒上发生的反应为:O2+2H2O+4e-→4OH- |
| C、若往溶液中加少许硫酸,无论a和b是否连接,铁片均会溶解,溶液逐渐变成浅绿色 |
| D、若氯化钠溶液改为氯化铵溶液,a和b连接,碳棒上有气泡产生 |
标准状况下H2和Cl2组成的混合气体a mol,其中氯气的体积分数为w.经光照后缓缓通入含b mol NaOH的溶液中充分反应,测得最终溶液中含有c mol NaClO(c>0),则下列说法正确的是( )
A、若c>b-a,则w=1-
| ||
B、若a+c>b,则w=1-
| ||
| C、若b=a+c,则w=0.5 | ||
D、若a<b-c,则w=
|
 如图是铅蓄电池充、放电时的工作示意图,电解质是H2SO4溶液.已知放电时电池反应为:Pb+PbO2+4H++2SO42-=2PbSO4+2H2O,下列有关说法正确的是( )
如图是铅蓄电池充、放电时的工作示意图,电解质是H2SO4溶液.已知放电时电池反应为:Pb+PbO2+4H++2SO42-=2PbSO4+2H2O,下列有关说法正确的是( )| A、K与N相接时,能量由电能转化为化学能 |
| B、K与N相接时,H+向Pb电极区迁移 |
| C、K与M连接时,所用电源的a极为正极 |
| D、K与M相接时,阳极附近的pH逐渐减小 |
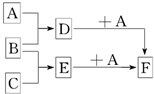 已知A、B、C是三种常见的单质,其中A为固体,B、C为气体;D的饱和溶液滴入沸水中继续煮沸,溶液呈红褐色;B和C反应的产物极易溶于水得无色溶液E.它们之间转化关系如图所示.
已知A、B、C是三种常见的单质,其中A为固体,B、C为气体;D的饱和溶液滴入沸水中继续煮沸,溶液呈红褐色;B和C反应的产物极易溶于水得无色溶液E.它们之间转化关系如图所示.