题目内容
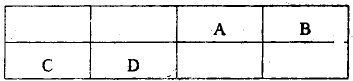
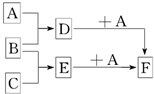 已知A、B、C是三种常见的单质,其中A为固体,B、C为气体;D的饱和溶液滴入沸水中继续煮沸,溶液呈红褐色;B和C反应的产物极易溶于水得无色溶液E.它们之间转化关系如图所示.
已知A、B、C是三种常见的单质,其中A为固体,B、C为气体;D的饱和溶液滴入沸水中继续煮沸,溶液呈红褐色;B和C反应的产物极易溶于水得无色溶液E.它们之间转化关系如图所示.(1)写出D和E分别与A反应的离子方程式:D+A:
(2)写出在F中加入NaOH并在空气中放置所发生的反应的化学方程式:
考点:无机物的推断,常见金属元素的单质及其化合物的综合应用
专题:推断题,几种重要的金属及其化合物
分析:A与B反应生成D,D的饱和溶液滴入沸水中继续煮沸,溶液呈红褐色,则D是氯化铁,A、B都是单质,且A是固体,所以A是铁,B是氯气;B和C反应生成E,E极易溶于水得无色溶液E,则C是氢气,E是氯化氢,盐酸和铁反应生成氯化亚铁与氢气,符合转化关系,则F是氯化亚铁,以此解答该题.
解答:
解:A与B反应生成D,D的饱和溶液滴入沸水中继续煮沸,溶液呈红褐色,则D是氯化铁,A、B都是单质,且A是固体,所以A是铁,B是氯气;B和C反应生成E,E极易溶于水得无色溶液E,则C是氢气,E是氯化氢,盐酸和铁反应生成氯化亚铁与氢气,符合转化关系,则F是氯化亚铁,
(1)D+A的反应为FeCl3和Fe的反应,反应的离子方程式为2Fe3++Fe═3Fe2+,盐酸和铁反应生成FeCl2,离子方程式为Fe+2H+═Fe2++H2↑,
故答案为:2Fe3++Fe═3Fe2+;Fe+2H+═Fe2++H2↑;
(2)F为FeCl2,加入氢氧化钠生成Fe(OH)2白色沉淀,反应的化学方程式为FeCl2+2NaOH═Fe(OH)2↓+2NaCl,Fe(OH)2不稳定,易被空气中的氧气氧化生成Fe(OH)3,方程式为4Fe(OH)2+O2+2H2O═4Fe(OH)3,
故答案为:FeCl2+2NaOH═Fe(OH)2↓+2NaCl、4Fe(OH)2+O2+2H2O═4Fe(OH)3.
(1)D+A的反应为FeCl3和Fe的反应,反应的离子方程式为2Fe3++Fe═3Fe2+,盐酸和铁反应生成FeCl2,离子方程式为Fe+2H+═Fe2++H2↑,
故答案为:2Fe3++Fe═3Fe2+;Fe+2H+═Fe2++H2↑;
(2)F为FeCl2,加入氢氧化钠生成Fe(OH)2白色沉淀,反应的化学方程式为FeCl2+2NaOH═Fe(OH)2↓+2NaCl,Fe(OH)2不稳定,易被空气中的氧气氧化生成Fe(OH)3,方程式为4Fe(OH)2+O2+2H2O═4Fe(OH)3,
故答案为:FeCl2+2NaOH═Fe(OH)2↓+2NaCl、4Fe(OH)2+O2+2H2O═4Fe(OH)3.
点评:本题考查物质的推断,为高频考点,侧重于学生的分析能力的考查,“D的饱和溶液滴入沸水中继续煮沸,溶液呈红褐色”是突破口,明确物质的性质及特殊性是解本题关键,难度不大.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案
相关题目
有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同.下列各项事实不能说明上述观点的是( )
| A、甲苯能使酸性高锰酸钾溶液褪色,而甲烷不能使高锰酸钾酸性溶液褪色 |
| B、乙烯能发生加成反应,而乙烷不能发生加成反应 |
| C、苯酚能和氢氧化钠溶液反应,而乙醛不能和氢氧化钠溶液反应 |
| D、苯酚苯环上的氢比苯分子中的氢更容易被卤原子取代 |
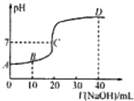 25℃时,用浓度为0.1000mol/L的NaOH溶液滴定20.00mL 0.1000mol/L的CH3COOH.滴定曲线如图所示.下列分析错误的是( )
25℃时,用浓度为0.1000mol/L的NaOH溶液滴定20.00mL 0.1000mol/L的CH3COOH.滴定曲线如图所示.下列分析错误的是( )| A、C点的溶液:c(CH3COO-)+c(CH3COOH)>c(Na-) |
| B、B点的溶液:c(CH3COO-)>(Na+)>c(H-)>c(OH-) |
| C、A点的纵坐标值为1 |
| D、D点溶液2c(CH3COOH)+c(H+)=c(OH-)-c(CH3COO-) |
下列实验现象所对应的离子方程式不正确的是( )
| A、向NaAlO2溶液中通入过量CO2:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3 |
| B、向Ba(OH)2溶液中加入稀H2SO4恰好完全反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
| C、向稀NaOH溶液氯水中加入:Cl2+2OH-═Cl-+ClO-+H2O |
| D、向FeCl2溶液中加入少量K3[Fe(CN)3]溶液:3Fe2++2[Fe(CN)3]3-═Fe3[Fe(CN)2]2↓ |