题目内容
【题目】为探究外界条件对可逆反应:2NO2(g) ![]() 2NO(g) +O2(g) ΔH=- 1162kJ·mol-1的影响,若保持气体的总质量不变,在温度为T1、T2时,通过实验得到平衡体系中 NO体积分数随压强的变化曲线,实验结果如图所示。下列说法正确的是( ):
2NO(g) +O2(g) ΔH=- 1162kJ·mol-1的影响,若保持气体的总质量不变,在温度为T1、T2时,通过实验得到平衡体系中 NO体积分数随压强的变化曲线,实验结果如图所示。下列说法正确的是( ):

A. a、c两点混合气体的平均相对分子质量:Ma>Mc
B. b、c两点的平衡常数:Kb=Kc
C. 从状态a到状态c,NO2气体的转化率减小
D. 状态a通过升高温度可变成状态b,a、b两点气体颜色:a深、b浅
【答案】C
【解析】
A.平均相对分子质量![]() ,m总不变。a、c两点所处的环境温度相同,压强不同,P2>P1。从a到c,增大压强,平衡向着气体体积减小的方向移动,即向逆反应方向移动,n总减小。根据公式平
,m总不变。a、c两点所处的环境温度相同,压强不同,P2>P1。从a到c,增大压强,平衡向着气体体积减小的方向移动,即向逆反应方向移动,n总减小。根据公式平![]() ,m总不变,n总减小,可得平均相对分子质量变大,有Ma<Mc,A项错误;
,m总不变,n总减小,可得平均相对分子质量变大,有Ma<Mc,A项错误;
B.b、c两点所处环境的温度不同。温度不同,则平衡常数不同。a和c的温度相同,可以通过a和b的对比,知道T1和T2的大小关系。a、b两点所处的环境温度不同,压强相同,从T1到T2,VNO%增大,反应向正反应方向移动,为放热反应方向,则T1到T2,为降低温度。对于放热反应,降低温度,平衡常数变大,则Kb<Kc;B项错误;
C.从a到c,增大压强,平衡向着气体体积减小的方向移动,即向逆反应方向移动,NO2气体的转化率减小,C项正确;
D.a、b两点所处的环境温度不同,压强相同,从T1到T2,VNO%增大,反应向正反应方向移动,为放热反应方向,则T1到T2,为降低温度。但是状态a到状态b除了升高温度外,还需要保持压强不变。此外状态a和状态b相比较,在状态a下,VNO%较大, NO2较少,颜色比较浅。D项错误;
本题答案选C。

【题目】运用化学反应原理研究氮、硫单质及其化合物性质是一个重要的课题。回答下列问题:
(1)恒容密闭容器中,工业固氮:N2(g)+3H2(g) ![]() 2NH3(g)的平衡常数K值和温度关系如表:
2NH3(g)的平衡常数K值和温度关系如表:
温度/℃ | 25 | 200 | 300 | 400 | 450 |
K | 5108 | 1.0 | 0.86 | 0.507 | 0.152 |
①从上表列出数据分析,该反应为__________反应(填:“吸热”或“放热”)。
②有关工业合成氨的研究成果,曾于1918年、1931年、2007年三次荣膺诺贝尔奖。下列关于关于合成氨反应描述的图像中,不正确的是_________(填:字母选项)。
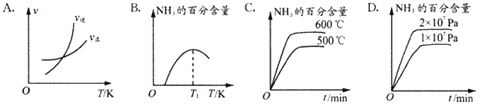
③450℃时,测得某时刻氨气、氮气、氢气物质的量浓度分别为3mol/L、2mol/L、1mol/L时,该反应的v(正)____________v(逆)(填“>”、“=”或“<”)。
(2)近年,科学家又提出在常温、常压、催化剂等条件下合成氨气的新思路,反应原理为:2N2(g)+6H2O(1)![]() 4NH3(g)+3O2(g),则其反应热ΔH=___________________。(已知:N2(g)+3H2(g)
4NH3(g)+3O2(g),则其反应热ΔH=___________________。(已知:N2(g)+3H2(g)![]() 2NH3(g) △H=-92.4kJ·mol-1 2H2(g) +O2(g)
2NH3(g) △H=-92.4kJ·mol-1 2H2(g) +O2(g)![]() 2H2O(l) △H=-571.6kJ·mol-1 )
2H2O(l) △H=-571.6kJ·mol-1 )
(3)联氨(N2H4)、二氧化氮(NO2)可与KOH溶液构成碱性燃料电池,其电池反应原理为2N2H4 +2NO2 = 3N2+8H2O。则负极的电极反应式为__________________________。
(4)部分金属硫化物的溶度积常数(Ksp)如下表:
硫化物 | CuS | ZnS | MnS | FeS |
Ksp | 6.3×10-36 | 2.9×10-25 | 2.5×10-13 | 6.3×10-18 |
由列表数据分析推知,向含有Cu2+、Zn2+、Mn2+、Fe2+的工业废水中加入MnS粉末的作用是_____________________________________。
(5)工业上从废铅蓄电池废液回收铅的过程中,常用纯碱溶液与处理后的铅膏(主要含PbSO4)发生反应:PbSO4(s)+CO32-(aq)![]() PbCO3(s)+SO42-(aq)。已知溶度积常数:Ksp(PbSO4)=1.6×10-8,Ksp(PbCO3)=7.4×10-14,则该反应的化学平衡常数K =_______。
PbCO3(s)+SO42-(aq)。已知溶度积常数:Ksp(PbSO4)=1.6×10-8,Ksp(PbCO3)=7.4×10-14,则该反应的化学平衡常数K =_______。