题目内容
1.已知元素的原子序数,可以推知原子的①原子数②核电荷数③核外电子数④在周期表中的位置,其中正确的是( )| A. | ①③ | B. | ②③ | C. | ①②③ | D. | ②③④ |
分析 由原子序数定义可直接得出②③;由③和核外电子排布规律可推原子结构示意图从而得出④,如:31号元素原子结构示意图为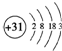 ,位于第四周期ⅢA族.
,位于第四周期ⅢA族.
解答 解:原子序数=质子数=核电核数=核外电子数,由核外电子数和核外电子排布规律可推可知原子结构示意图,由原子结构示意图可知元素在周期表中的位置,即由原子序数定义可以推知原子②③④,但无法得出原子数,故选D.
点评 本题考查原子结构知识,题目难度不大,本题注意把握相关知识的积累.

练习册系列答案
相关题目
11.下表列出了A~M 13种元素在周期表中的位置:
(1)这些元素中,金属性最强的元素是钾(填元素名称),非金属性最强的元素是氟(填元素名称),最不活泼的元素是Ar(填元素符号),原子半径最小的元素是H(填元素符号).
(2)写出C元素的气态氢化物与I元素的最高价氧化物的水化物反应的化学方程式:2NH3+H2SO4=(NH4)2SO4.
(3)将C、D、E三种元素的氢化物按还原性增强的顺序排列为HF<H2O<NH3.(用化学式表示)
(4)I2-、J-、L+、M2+等微粒中,半径最大的是S2-(填离子符号).
(5)A与D形成的化合物A2D2是共价化合物(填共价或离子),其电子式为 .
.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅤⅠA | ⅤⅡA | 0 |
| 1 | A | |||||||
| 2 | B | C | D | E | ||||
| 3 | F | G | H | I | J | K | ||
| 4 | L | M |
(2)写出C元素的气态氢化物与I元素的最高价氧化物的水化物反应的化学方程式:2NH3+H2SO4=(NH4)2SO4.
(3)将C、D、E三种元素的氢化物按还原性增强的顺序排列为HF<H2O<NH3.(用化学式表示)
(4)I2-、J-、L+、M2+等微粒中,半径最大的是S2-(填离子符号).
(5)A与D形成的化合物A2D2是共价化合物(填共价或离子),其电子式为
 .
.
12.下列对化合物M、N的叙述正确的是( )


| A. | M的分子式为C12H9O3 | |
| B. | 1mol M在最多能与6molH2发生加成反应 | |
| C. | M与N可用试剂组合:溴水、NaOH溶液鉴别 | |
| D. | M与N可用试剂组合:FeCl3溶液、稀H2SO4鉴别 |
9.常温下pH最小的是下列各项中的( )
| A. | pH=0的溶液 | B. | 0.04 mol•L-1H2SO4 | ||
| C. | 0.5 mol•L-1HCl | D. | 0.05 mol•L-1CH3COOH |
16.咖啡酸具有止血功效,存在于多种中药中,其结构简式如图:则下列有关说法正确的是( )
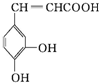

| A. | 该物质中苯环上一氯代物有2种 | |
| B. | 该分子结构中含有两种官能团 | |
| C. | 既能发生取代反应,也能发生加成反应 | |
| D. | 所有碳原子不可能都在同一个平面上 |
13.阿魏酸在食品、医药等方面有若干广泛用途.一种合成阿魏酸的反应可表示为
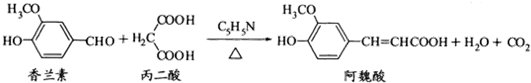
下列说法正确的是( )

下列说法正确的是( )
| A. | 可用酸性KMnO4溶液检测上述反应是否有阿魏酸生成 | |
| B. | 香兰素、阿魏酸均可与Na2CO3、NaOH、NaHCO3溶液反应 | |
| C. | 香兰素、阿魏酸都能发生取代、加成、消去反应 | |
| D. | 与香兰素互为同分异构体,分子中有4种不同化学环境的氢,且能发生银镜反应的酚类化合物共有2种 |
10.分类就是按照种类、等级或性质分别归类.依据不同的分类标准,结论也不尽相同.下列每组中有一种物质具有特殊的组成或性质,而其他两种物质的组成或性质相似.请你利用所学知识将其区分出来并说明理由.
| 化学式 | 被区分的物质(名称) | 理由 |
| Na2CO3、CaCO3、NaCl | NaCl | 由两种元素组成,或不含碳(或氧)元素 |
| C、CO2、H2CO3 | 碳 | 单质 |
11.下列属于共价化合物的是( )
| A. | Cl2 | B. | NaOH | C. | CH4 | D. | (NH4)2SO4 |
 I.
I.