题目内容
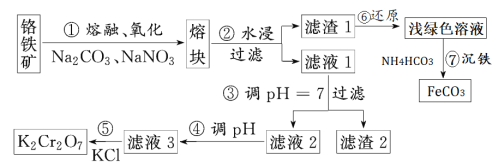
【题目】重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为FeO·Cr2O3,还含有硅、铝等杂质。制备流程如图所示:
回答下列问题:
(1)步骤①的主要反应为:FeO·Cr2O3+Na2CO3+NaNO3→Na2CrO4+Fe2O3+CO2+NaNO2。上述反应配平后NaNO3与FeO·Cr2O3与的系数比为___。该步骤不能使用陶瓷容器,原因是___。
(2)滤渣1中主要成分是___,滤渣2中含量最多的金属元素名称是___。
(3)步骤④调滤液2的pH变小的目的是___(用离子方程式表示)。
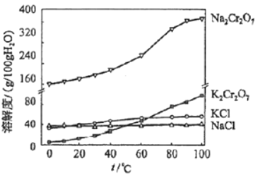
(4)有关物质的溶解度如图所示。向“滤液3”中加入适量KCl,___、___,过滤得到K2Cr2O7固体。该反应的反应类型是___。
(5)写出步骤7中涉及的离子方程式___。
【答案】7:2 陶瓷在高温下会与Na2CO3反应 Fe2O3 铝 增大溶液中H+,促进平衡2CrO42-+2H+Cr2O72-+H2O正向移动 蒸发浓缩 冷却结晶 复分解反应 Fe2++2HCO3-=FeCO3↓+CO2↑+H2O
【解析】
铬铁矿的主要成分为FeOCr2O3,还含有硅、铝等杂质,制备重铬酸钾,由制备流程可知,步骤①的主要反应为FeO·Cr2O3+Na2CO3+NaNO3=Na2CrO4+Fe2O3+CO2+NaNO2,Cr元素的化合价由+3价升高为+6价,Fe元素的化合价由+2价升高为+3价,N元素的化合价由+5价降低为+3价,由电子、原子守恒可知,反应为2FeOCr2O3+4Na2CO3+7NaNO3![]() 4Na2CrO4+Fe2O3+4CO2+7NaNO2,该步骤中若使用陶瓷,二氧化硅与碳酸钠高温下反应生成硅酸钠和二氧化碳,则使用铁坩埚,熔块水浸过滤分离出滤渣1含Fe2O3,经还原可制备碳酸亚铁,滤液1中含NaAlO2、Na2CrO4、硅酸钠,调节pH=7,SiO32-离子转化为H2SiO3,AlO2-转化为Al(OH)3,过滤分离出Al(OH)3、H2SiO3,滤液2中含Na2CrO4,④中调节pH发生2CrO42-+2H+Cr2O72-+H2O,滤液3含Na2Cr2O7,由水中的溶解度:Na2Cr2O7>K2Cr2O7,可知⑤中向Na2Cr2O7溶液中加入KCl固体后得到K2Cr2O7,溶解度小的析出,以此解答该题。
4Na2CrO4+Fe2O3+4CO2+7NaNO2,该步骤中若使用陶瓷,二氧化硅与碳酸钠高温下反应生成硅酸钠和二氧化碳,则使用铁坩埚,熔块水浸过滤分离出滤渣1含Fe2O3,经还原可制备碳酸亚铁,滤液1中含NaAlO2、Na2CrO4、硅酸钠,调节pH=7,SiO32-离子转化为H2SiO3,AlO2-转化为Al(OH)3,过滤分离出Al(OH)3、H2SiO3,滤液2中含Na2CrO4,④中调节pH发生2CrO42-+2H+Cr2O72-+H2O,滤液3含Na2Cr2O7,由水中的溶解度:Na2Cr2O7>K2Cr2O7,可知⑤中向Na2Cr2O7溶液中加入KCl固体后得到K2Cr2O7,溶解度小的析出,以此解答该题。
(1)由上述分析可知步骤①的主要反应为2FeOCr2O3+4Na2CO3+7NaNO3![]() 4Na2CrO4+Fe2O3+4CO2+7NaNO2,则NaNO3与FeOCr2O3与的系数比为7:2;该步骤不能使用陶瓷容器,原因是二氧化硅与碳酸钠高温下反应生成硅酸钠和二氧化碳;
4Na2CrO4+Fe2O3+4CO2+7NaNO2,则NaNO3与FeOCr2O3与的系数比为7:2;该步骤不能使用陶瓷容器,原因是二氧化硅与碳酸钠高温下反应生成硅酸钠和二氧化碳;
(2)由以上分析可知滤渣1含Fe2O3,滤渣2含有Al(OH)3、H2SiO3,滤渣中含量最多的金属元素是铝元素;
(3)④中调节pH发生2CrO42+2H+Cr2O72+H2O,则步骤④调滤液2的pH使之变小,增大氢离子浓度,平衡正向移动,利于生成Cr2O72;
(4)向“滤液3”中加入适量KCl,蒸发浓缩,冷却结晶,过滤得到K2Cr2O7固体,步骤⑤发生Na2Cr2O7+2KCl=K2Cr2O7↓+2NaCl,反应类型是复分解反应;
(5)步骤7中涉及的离子方程式为Fe2++2HCO3-=FeCO3↓+CO2↑+H2O。