题目内容
【题目】A、B、C、D、E、F属于短周期主族元素。已知A元素原子是短周期元素原子中半径最大的原子;B元素原子是其中原子半径最小的原子;C元素原子的最外层电子数为m,次外层电子数为n;D元素原子的L层电子数为m+n,M层电子数为m-n;E元素原子的最外层电子数等于其电子层数,且在周期表中与D元素相邻;F元素原子的核外电子数是C元素原子的2倍;A、B、C三种元素可组成化合物X,C、E可组成化合物Y。
(1)D的元素符号为____,F原子的结构示意图为______,X的电子式是_______,D、C形成的是_______(填“共价”或“离子”)化合物。
(2)A~F所形成的与氖原子具有相同电子层结构的简单离子半径由大到小的顺序是______ (用离子符号表示)。
(3)化合物Y与X的水溶液反应的离子方程式为________________。
【答案】Si 
![]() 共价 O2>Na+>Al3+ Al2O3+2OH-=2AlO2-+H2O
共价 O2>Na+>Al3+ Al2O3+2OH-=2AlO2-+H2O
【解析】
A、B、C、D、E、F属于短周期主族元素,其中A元素原子是短周期中原子半径最大的原子,则A为Na元素;B是最小的原子,则B为H元素;C元素原子的最外层电子数为m,次外层电子数为n;D元素原子的L层电子数为m+n,M层电子数为m-n,则m+n=8,故C元素原子的次外层为第1电子层,则n=2,故m=6,则C为氧元素,D最外层电子数为6-2=4,则D为Si元素;E元素原子的最外层电子数等于其电子层数,则最外层电子数为3,故E为Al元素;F元素原子的核外电子数是C元素原子的2倍,则F原子核外电子数为16,故F为硫元素。A、B、C三种元素可组成化合物X为NaOH,C、E可组成化合物Y为Al2O3,据此解答。
(1)D为硅,元素符号为Si,F为硫元素,原子的结构示意图为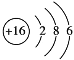 ,X为NaOH,其电子式是
,X为NaOH,其电子式是![]() ,D、C形成的二氧化硅是共价化合物;
,D、C形成的二氧化硅是共价化合物;
(2)具有相同电子层结构的离子,核电荷数越大半径越小,故A~F所形成的与氖原子具有相同电子层结构的简单离子半径由大到小的顺序是O2>Na+>Al3+;
(3)化合物Y(Al2O3)与X(NaOH)的水溶液反应生成偏铝酸钠和水,反应的离子方程式为Al2O3+2OH-=2AlO2-+H2O。

 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案【题目】下列有关实验现象、解释和结论都正确的是
选项 | 实验操作 | 实验现象 | 解释或结论 |
A | 将充满NO2的密闭玻璃球浸泡在热水中 | 红棕色变深 | 反应2NO2 |
B | 等体积pH=2的HX和HY两种酸分别与足量的铁反应,用排水法收集气体 | HX放出的氢气多且反应速率快 | 酸的强弱:HX<HY |
C | 常温下,用pH计分别测定0.1moI/LNaA溶液的0.1moI/LNaB溶液的pH | pH:NaA>NaB | 能证明酸性:HA>HB |
D | 向盛有1mL0.lmol/L的AgNO3溶液中加入10滴0.1mol/L的NaCl溶液,振荡,再加入10滴0.1mol/L的NaI溶液,再振荡, | 先生成白色沉淀,后产生黄色沉淀 | Ksp(AgI)<Ksp(AgCl) |
A.AB.BC.CD.D
【题目】实验室以蛇纹石酸浸出液![]() 主要含
主要含![]() ,还有一定量的
,还有一定量的![]() 、
、![]() 、
、![]() 、
、![]() 等
等![]() 为原料制备高纯氧化铁,流程如图1:
为原料制备高纯氧化铁,流程如图1:
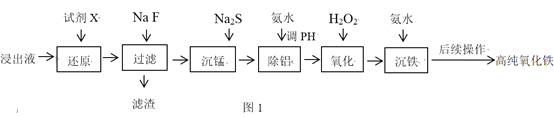
已知流程中相关金属离子生成氢氧化物沉淀的pH如表:
氢氧化物 |
|
|
|
开始沉淀的pH |
|
|
|
沉淀完全的pH |
|
|
|
已知:在该温度下,Ksp(CaF2)=2.0×10-10 Ksp(MnF2)=5.0×10-3 Ksp(MgF2)=7.4×10-11
(1)“还原”时,应选择______![]() 填字母
填字母![]() .
.
A.Zn粉![]() 溶液
溶液![]() 粉
粉
(2)“滤渣”的主要成分除含有少量![]() 外,还含有______
外,还含有______![]() 填化学式
填化学式![]() .
.
(3)“沉锰”时,已知:![]() 为确保沉锰完全
为确保沉锰完全![]() 即溶液中
即溶液中![]() ,应保持溶液中
,应保持溶液中![]() ______
______![]() .
.
(4)“除铝”时,控制溶液pH的范围为_____________
(5)“氧化”时,常用酸性![]() 溶液检测是否残留未被氧化的金属离子,该反应的离子方程式为__________
溶液检测是否残留未被氧化的金属离子,该反应的离子方程式为__________
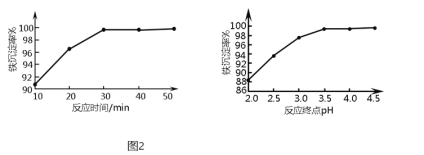
(6)“沉铁”时,反应温度为![]() 条件下,反应时间和反应终点pH对铁的沉淀率的影响分别如图2所示,则最佳的工艺条件是______.
条件下,反应时间和反应终点pH对铁的沉淀率的影响分别如图2所示,则最佳的工艺条件是______.
【题目】“84消毒液”因1984年北京某医院研制使用而得名,在日常生活中使用广泛,其有效成分是NaClO。某小组在实验室制备NaClO溶液,并进行性质探究和成分测定。
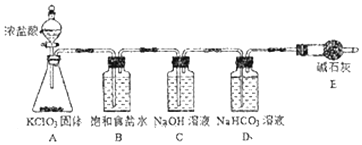
(1)该小组按如图装置进行实验,反应一段时间后,分别取B、C、D瓶的溶液进行实验,实验现象如表。(已知饱和NaClO溶液pH为11)
实验步骤 | 实验现象 | ||
B瓶 | C瓶 | D瓶 | |
实验1:取样,滴加紫色石蕊溶液 | 变红,缓慢褪色 | 变红,缓慢褪色 | 立即褪色 |
实验2:取样,测定溶液的pH | 3 | 12 | 7 |
①装置A中反应的化学方程式为____。
②B瓶溶液中H+的主要来源是____。
③C瓶溶液的溶质是___(填化学式)。
④结合平衡移动原理解释D瓶溶液中石蕊立即褪色的原因____。
(2)测定C瓶溶液中NaClO含量(单位:gL-1)的实验步骤如下:
Ⅰ.取C瓶溶液20mL于锥形瓶,加足量盐酸酸化,迅速加入过量KI溶液,盖紧瓶塞并在暗处充分反应。
Ⅱ.用0.1000molL-1Na2S2O3标准溶液滴定锥形瓶中的溶液,指示剂显示终点时共用去20.00mLNa2S2O3溶液。(I2+2S2O32-=2I-+S4O62-)
①NaClO的电子式为____。
②步骤Ⅰ总反应的离子方程式为____。
③C瓶溶液中NaClO的含量为____gL-1。(保留1位小数,NaClO式量为74.5)