题目内容
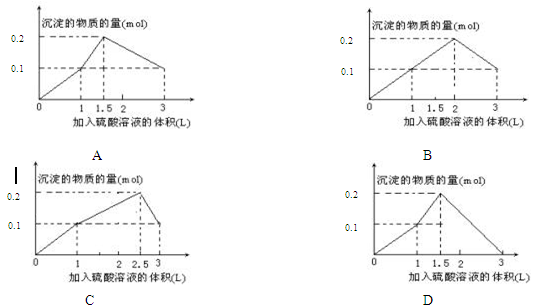
将Na2O2逐渐加入到含有Al3+、Mg2+、NH4+的混合溶液中并加热,产生沉淀和气体的物质的量与加入Na2O2的物质的量的关系如图所示。

则原溶液中Al3+、Mg2+、NH4+的物质的量分别为 ( )

则原溶液中Al3+、Mg2+、NH4+的物质的量分别为 ( )
| A.2 mol、3 mol、8 mol | B.3 mol、2 mol、8 mol |
| C.2 mol、3 mol、4 mol | D.3 mol、2 mol、4 mol |
C
加入8molNa2O2时,根据钠原子守恒,可知n(Na+)=2n(Na2O2)=2×8mol=16mol,Na+离子所带的总电量相当于16mol×1=16mol.
A、Al3+、Mg2+、NH4+离子所带的总电量相当于2mol×3+3mol×2+8mol×1=20mol,故A错误;
B、Al3+、Mg2+、NH4+离子所带的总电量相当于3mol×3+2mol×2+8mol×1=21mol,故B错误;
C、Al3+、Mg2+、NH4+离子所带的总电量相当于2mol×3+3mol×2+4mol×1=16mol,故C正确;
D、Al3+、Mg2+、NH4+离子所带的总电量相当于3mol×3+2mol×2+4mol×1=17mol,故D错误.
故选C.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目