题目内容
 某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物物质,其实验装置如图.加热聚丙烯废塑料得到的产物如下表:
某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物物质,其实验装置如图.加热聚丙烯废塑料得到的产物如下表:| 产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
| 质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |
| ① |
| ② |
| ③ |
(2)试管B收集到的两种产品中,有一种能使酸性高锰酸钾溶液褪色的物质,其一氯代物有
(3)锥形瓶C中观察到的现象
考点:常用合成高分子材料的化学成分及其性能
专题:有机化合物的获得与应用
分析:(1)电石为碳化钙与水反应生成乙炔;乙炔含有碳碳三键能够加聚生成聚乙炔;
(2)能使酸性高锰酸钾溶液褪色的物质有乙烯、丙烯和甲苯,但是只有甲苯在0度是液态,依据甲苯中含不同氢原子种数判断一氯代物的种数;
(3)乙烯、丙烯均含有碳碳双键能够与溴发生加成反应.
(2)能使酸性高锰酸钾溶液褪色的物质有乙烯、丙烯和甲苯,但是只有甲苯在0度是液态,依据甲苯中含不同氢原子种数判断一氯代物的种数;
(3)乙烯、丙烯均含有碳碳双键能够与溴发生加成反应.
解答:
解:(1)电石制备乙炔的方程式为:CaC2+2H2O=Ca(OH)2+C2H2↑;乙炔加聚生成聚乙炔的化学方程式为:nC2H2→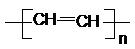 ;
;
故答案为:CaC2+2H2O=Ca(OH)2+C2H2↑;
(2)甲苯常温下是液态,能够使酸性的高锰酸钾褪色,甲苯中苯环上的一氯代物有3种,甲基上的一氯代物有1种,所以一氯代物共有4种;
故答案为:4;
(3)乙烯、丙烯均含有碳碳双键能够与溴发生加成反应,所以C中可以看到的现象是溶液褪色;
故答案为:溶液褪色.
故答案为:CaC2+2H2O=Ca(OH)2+C2H2↑;
(2)甲苯常温下是液态,能够使酸性的高锰酸钾褪色,甲苯中苯环上的一氯代物有3种,甲基上的一氯代物有1种,所以一氯代物共有4种;
故答案为:4;
(3)乙烯、丙烯均含有碳碳双键能够与溴发生加成反应,所以C中可以看到的现象是溶液褪色;
故答案为:溶液褪色.
点评:本题考查了常见有机物的结构和性质,属于物质结构和性质是解题关键,注意对课本基础知识的巩固,题目难度不大.

练习册系列答案
相关题目
在约100℃的温度下,NaCl稀溶液中[H+]为1×10-6 mol?L-1.下列说法中正确的是( )
| A、该NaCl溶液显酸性 |
| B、该NaCl溶液显碱性 |
| C、该NaCl溶液中KW=1×10-14mol2?L-2 |
| D、该NaCl溶液中KW=1×10-12mol2?L-2 |
下列说法中,能够判断一个反应是否是氧化还原反应的是( )
| A、反应前后,元素是否有电子转移 |
| B、反应前后,元素是否有化合价变化 |
| C、反应前后,是否有氧元素参加 |
| D、反应前后,是否有氢元素参加 |
某种橡胶的分解产物为碳氢化合物,对这种碳氢化合物作如下实验:①若取一定量完全燃烧,使燃烧后的气体通过干燥管,干燥管增重0.72g,再通过石灰水,石灰水增重2.2g.②经测定,该碳氢化合物(气体)的密度是相同条件下氢气密度的34倍.③该碳氢化合物0.1mol能和32g溴起加成反应.④经分析,在③的生成物中,溴原子分布在不同的碳原子上,且溴代物中有一个碳原子在支链上.下列说法正确的是( )
| A、该碳氢化合物为2-甲基-1,3-戊二烯 |
| B、该碳氢化合物与溴单质1:1加成时可以生成3种不同的产物 |
| C、该碳氢化合物与溴单质1:1加成时可以生成2种不同的产物 |
| D、该碳氢化合物与足量氢气加成时可以生成正戊烷 |
正确掌握化学用语和化学基本概念是学好化学的基础.下列有关表述中正确的一组是( )
| A、16O与18O互为同位素;H216O、D216O、H218O、D218O互为同素异形体 |
| B、SiH4、PH3、HCl的稳定性逐渐增强 |
| C、氧化铁的化学式:FeO |
D、Ca2+的结构示意图为 ,NH4Cl的电子式为 ,NH4Cl的电子式为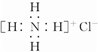 |