��Ŀ����
����Ŀ��1��6�������ᣨG���Ǻϳ���������Ҫԭ��֮һ�����ú�����̼ԭ�ӵ��л������������Ʊ�����ͼΪAͨ��������Ӧ�Ʊ�G�ķ�Ӧ���̣����ܵķ�Ӧ�м�����ΪB��C��D��E��F���� 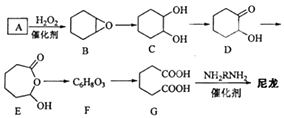
��1��������A�к�̼87.8%������Ϊ�⣬A�Ļ�ѧ����Ϊ ��
��2��C��D �ķ�Ӧ����Ϊ ��
��3��F�Ľṹ��ʽΪ ��
��4��B��C��D�����м������У��˴Ź������׳��������� �� ���ٵ��� ��
��5��������һ���л��߷��ӻ������G�ϳ������Ļ�ѧ����ʽΪ ��
��6����Aͨ��������Ӧ�Ʊ�1��3��������ϩ�ĺϳ�·��Ϊ ��
���𰸡�
��1������ϩ
��2��������Ӧ
��3��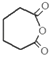
��4��D��B
��5��![]()
��6��![]()
![]()
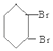
![]()
![]()
���������⣺������A�к�̼87.8%������Ϊ�⣬��̼��ԭ�Ӹ�����Ϊ�� ![]() ��
�� ![]() =6��10����֪A��������̼ԭ�ӣ���A�ķ���ʽ��C6H10 �� A�ṹ��ʽΪ
=6��10����֪A��������̼ԭ�ӣ���A�ķ���ʽ��C6H10 �� A�ṹ��ʽΪ ![]() ��˫��ˮ��Ӧ����
��˫��ˮ��Ӧ���� ![]() ��
�� ![]() ��ˮ�����ӳɷ�Ӧ����
��ˮ�����ӳɷ�Ӧ���� ![]() ��
�� ![]() ����������Ӧ����
����������Ӧ���� ![]() ��
�� ![]() �ٷ���������Ӧ����
�ٷ���������Ӧ���� 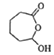 ��
�� 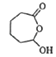 �ٷ���������Ӧ����F��FΪ��
�ٷ���������Ӧ����F��FΪ�� ![]() ��
�� ![]() �ٷ���������Ӧ����
�ٷ���������Ӧ���� ![]() ��
�� ![]() ��
�� ![]() �������۷�Ӧ������������ѧʽΪ��
�������۷�Ӧ������������ѧʽΪ�� ![]() ����1��A�ṹ��ʽΪ
����1��A�ṹ��ʽΪ ![]() ������Ϊ����ϩ�����Դ��ǣ�����ϩ����2��C����������Ӧ����D�����Դ��ǣ�������Ӧ����3��ͨ�����Ϸ���֪��FΪ��
������Ϊ����ϩ�����Դ��ǣ�����ϩ����2��C����������Ӧ����D�����Դ��ǣ�������Ӧ����3��ͨ�����Ϸ���֪��FΪ�� ![]() �����Դ��ǣ�
�����Դ��ǣ� ![]() ����4���˴Ź�������������ԭ��������ͬ����ԭ������Խ����˴Ź���������Խ�࣬B�ĺ˴Ź������׳���Ϊ3��C�ĺ˴Ź������׳���Ϊ4��D�ĺ˴Ź������׳���Ϊ6��E�ĺ˴Ź������׳���Ϊ6��F�ĺ˴Ź������׳���Ϊ2������BCD�к˴Ź���������������D�����ٵ���B�����Դ��ǣ�D��B����5��G�ϳ������ķ���ʽΪ
����4���˴Ź�������������ԭ��������ͬ����ԭ������Խ����˴Ź���������Խ�࣬B�ĺ˴Ź������׳���Ϊ3��C�ĺ˴Ź������׳���Ϊ4��D�ĺ˴Ź������׳���Ϊ6��E�ĺ˴Ź������׳���Ϊ6��F�ĺ˴Ź������׳���Ϊ2������BCD�к˴Ź���������������D�����ٵ���B�����Դ��ǣ�D��B����5��G�ϳ������ķ���ʽΪ ![]() ��
��
���Դ��ǣ� ![]() ����6��A���巢���ӳɷ�Ӧ����
����6��A���巢���ӳɷ�Ӧ���� ![]() ��
�� 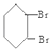 ������ȥ��Ӧ����
������ȥ��Ӧ���� ![]() ��������ϳ�·��Ϊ
��������ϳ�·��Ϊ ![]()
![]()
![]()
![]()
![]() ��
��
���Դ��ǣ� ![]()
![]()

![]()
![]() ��
��

 �Ͻ�ƽСѧ��������ϵ�д�
�Ͻ�ƽСѧ��������ϵ�д� �Ƹ������������ϵ�д�
�Ƹ������������ϵ�д�����Ŀ��Ϊ��̽��H2O2��H2SO3��Br2�����Ե����ǿ�����������ʵ�飨�г���������ȥ������ش��������⣺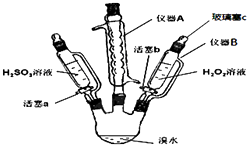
��1������A������ �� �������� ��
��2��������B�μ�Һ�岢����Ҫ������c��ԭ���� ��
��3��ʵ���¼���£��벹ȫ�հף���
���� | ʵ����� | ʵ������ | ʵ����� |
�� | ����a����μ���H2SO3��Һ������ | ||
�� | �����������Һ����μ���H2O2��Һ | �տ�ʼ��Һ��ɫ�����Ա仯�������μӣ���Һ��Ϊ�Ȼ�ɫ |
��4��������У���ʼʱ��ɫ�����Ա仯��ԭ���ǣ�д��һ���� �� ������з�Ӧ�����ӷ���ʽ ��
���������Ҫ��Ӧ�����ӷ���ʽ ��
