题目内容
8.下列物质中,含有共价键的离子晶体是( )| A. | KBr | B. | HCl | C. | I2 | D. | NaOH |
分析 活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,含有离子键的化合物是离子化合物,离子化合物中可能含有共价键.
解答 解:A.KBr中只含离子键,为离子化合物,故A错误;
B.HCl中H-Cl原子之间只存在共价键,为共价化合物,故B错误;
C.碘分子中I-I原子之间只存在共价键,为单质,故C错误;
D.NaOH中钠离子和氢氧根离子之间存在离子键、O-H原子之间存在共价键,为离子化合物,故D正确;
故选D.
点评 本题考查离子键和共价键判断,为高频考点,侧重考查基本概念,明确离子键和共价键根本区别是解本题关键,注意不能根据是否含有金属元素判断离子键,为易错点.

练习册系列答案
 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案
相关题目
3.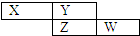 X、Y、Z、W均为短周期元素,它们在周期表的位置如图所示,若W原子的最外层电子数是内层电子总数的$\frac{7}{10}$,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表的位置如图所示,若W原子的最外层电子数是内层电子总数的$\frac{7}{10}$,下列说法中正确的是( )
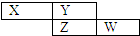 X、Y、Z、W均为短周期元素,它们在周期表的位置如图所示,若W原子的最外层电子数是内层电子总数的$\frac{7}{10}$,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表的位置如图所示,若W原子的最外层电子数是内层电子总数的$\frac{7}{10}$,下列说法中正确的是( )| A. | 阴离子的半径从大到小排列顺序为:X>Y>Z>W | |
| B. | X元素的氢化物分子间可以形成氢键 | |
| C. | Y的两种同素异形体在常温下可以相互转化 | |
| D. | 最高价氧化物对应的水化物的酸性:W>Z |
13.下列各组气体中,在通常情况下能共存,并且既能用浓硫酸又能用碱石灰干燥的是( )
| A. | SO2、H2S、O2 | B. | CH4、H2、O2 | C. | C2H4、N2、NH3 | D. | HCl、C12、CO2 |
20.在一定温度下,容积一定的密闭容器中发生反应A(s)+2B(g)?C(g)+D(g),当下列物理量不再发生变化时,表明反应已达平衡的是( )
①混合气体的密度②混合气体的压强③B的物质的量浓度④混合气体的总物质的量.
①混合气体的密度②混合气体的压强③B的物质的量浓度④混合气体的总物质的量.
| A. | ①② | B. | ②③ | C. | ①③ | D. | ①④ |
17.下列说法正确的是( )
| A. | 单位体积溶液里所含的溶质的物质的量,叫做物质的量浓度 | |
| B. | 气体摩尔体积就是22.4L mol- | |
| C. | 摩尔质量就是微粒的相对分子质量或者相对原子质量 | |
| D. | 物质的量就是物质的质量 |
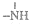 ,
,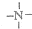 一定条件下都可以和H+结合.则N4和足量的H+反应生成的粒子的化学式为N4H44+.
一定条件下都可以和H+结合.则N4和足量的H+反应生成的粒子的化学式为N4H44+. .
.