题目内容
实验室欲快速制取H2,应选用正确的措施是( )
| A、纯锌与稀硫酸反应 |
| B、粗锌跟浓硫酸反应 |
| C、粗锌跟稀硝酸反应 |
| D、将浸泡过CuSO4溶液的锌跟稀硫酸反应 |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:快速制取氢气,可用粗锌和稀硫酸反应,浓硫酸和稀硝酸都不能与锌反应生成氢气.
解答:
解:浓硫酸和稀硝酸都不能与锌反应生成氢气,
实验室制备氢气应用稀硫酸,
A与D相比较,D易形成原电池反应而导致反应速率加快,
则应用浸泡过CuSO4溶液的锌跟稀硫酸反应,
故选D.
实验室制备氢气应用稀硫酸,
A与D相比较,D易形成原电池反应而导致反应速率加快,
则应用浸泡过CuSO4溶液的锌跟稀硫酸反应,
故选D.
点评:本题较简单,考查影响化学反应速率的常见因素,为高频考点,侧重于学生的分析能力的考查,学生应熟悉温度、浓度、构成原电池、增大接触面等对化学反应速率的影响来解答,但浓硫酸、硝酸的性质是学生解答中容易忽略的知识.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
葡萄糖是一种单糖的主要原因是( )
| A、在糖类结构中最简单 |
| B、不能再水解生成更简单的糖 |
| C、分子中含有一个醛基 |
| D、在所有糖类中碳原子数最少 |
绿原酸的结构简式如图,下列有关绿原酸的说法不正确的是( )
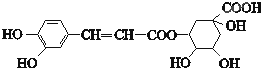
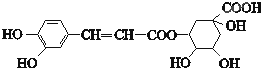
| A、分子式为C16H18O9 |
| B、0.1mol绿原酸最多与0.8mol NaOH反应 |
| C、能发生取代反应和消去反应 |
| D、能与Na2CO3反应 |
下列各组离子在溶液中因发生氧化还原反应而不能大量共存的是( )
| A、H+、NO3-、Fe2+、Na+ |
| B、K+、Ba2+、OH-、SO42- |
| C、Fe2+、NO3-、I-、K+ |
| D、Cu2+、NH4+、Cl-、OH- |
下列用来表示物质变化的化学用语中,正确的是( )
| A、明矾水解的离子方程式:Al3++3H2O?Al(OH)3↓+3H+ | ||||
| B、电镀时,要在铁上镀银,则正极为银,电极反应式为:Ag++e-═Ag | ||||
C、以石墨作电极电解氯化镁溶液:2Cl-+2H2O
| ||||
D、表示氢气燃烧热的化学方程式:H2(g)+
|
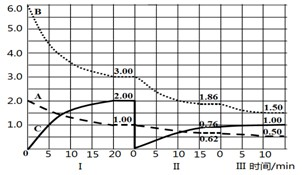 反应aA(g)+bB(g)?cC(g)(△H<0)在等容条件下进行.改变其它反应条件,在I、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图所示,下列说法不正确的是( )
反应aA(g)+bB(g)?cC(g)(△H<0)在等容条件下进行.改变其它反应条件,在I、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图所示,下列说法不正确的是( )| A、反应的化学方程式中,a:b:c=1:3:2 |
| B、A的平均反应速率vⅠ(A)、vⅡ(A)、vⅢ(A),最大的是vⅠ(A) |
| C、第Ⅱ阶段反应温度小于第Ⅲ阶段反应温度 |
| D、由第一次平衡到第二次平衡,采取的措施是从反应体系中移走C |
下列反应的离子方程式书写正确的是( )
| A、少量SO2气体通入到NaClO溶液中:SO2+ClO-+H2O═SO42-+Cl-+2H+ |
| B、把Fe(OH)3溶于氢氟酸:Fe(OH)3+3H+═Fe3++3H2O |
| C、向H218O中投入Na2O2固体:2H218O+2Na2O2═4Na++4OH-+18O2↑ |
| D、在苯酚钠溶液中通入少量的二氧化碳气体:C6H5O-+CO2+H2O═C6H5OH+HCO3- |
X、Y、Z、R、W是五种短周期元素,原子序数依次增大;它们可组成离子化合物Z2Y和共价化合物RY3、XW4;已知Y、R同主族,Z、R、W同周期.下列说法错误的是( )
| A、原子半径:Z>R>W |
| B、气态氢化物稳定性:HW>H2R |
| C、XW4分子中各原子均满足8电子结构 |
| D、Y、Z、R三种元素组成的化合物水溶液一定显碱性 |
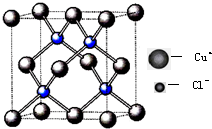 利用反应:Cu2Cl2+C2H2+2NH3→Cu2C2(乙炔亚铜,红色)+2NH4Cl可检验乙炔.
利用反应:Cu2Cl2+C2H2+2NH3→Cu2C2(乙炔亚铜,红色)+2NH4Cl可检验乙炔.