题目内容
6.有机物A的结构简式如下所示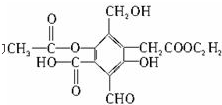
(1)A与过量NaOH完全反应时,A与参加反应的NaOH的物质的量之比为1:4.
(2)A与新制Cu(OH)2完全反应时,A与参加反应的Cu(OH)2物质的量之比为1:2,其中A与被还原的Cu(OH)2的物质的量之比为1:2.
(3)A与过量NaHCO3完全反应时,A与参加反应的NaHCO3物质的量之比为1:1.
分析 有机物含有酯基,可发生水解反应,含有酚羟基,可与氢氧化钠反应,含有羧基,具有酸性,可发生中和、酯化反应,以此解答该题.
解答 解:(1)能与NaOH反应的官能团有酯基、羧基和酚羟基,且1个酯基可水解生成乙酸和酚羟基,都能与NaOH反应,则A与参加反应的NaOH的物质的量之比为1:4,
故答案为:1:4;
(2)-COOH、-CHO与新制Cu(OH)2完全反应,1mol-COOH消耗0.5molCu(OH)2,1mol-CHO消耗2molCu(OH)2,被氧化生成的-COOH继续反应,只有与醛的反应为还原反应,则A与被还原的Cu(OH)2的物质的量之比为1:2,故答案为:1:2;1:2;
(3)能与碳酸氢钠反应的官能团只有羧基,A与参加反应的NaHCO3物质的量之比为1:1,故答案为:1:1.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团的性质为解答的关键,注意结构与性质的关系即可解答,题目难度中等.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
16.在光照下,将等物质的量的CH4和Cl2充分反应,得到产物的物质的量最多的是( )
| A. | HCl | B. | CH3Cl | C. | CHCl3 | D. | CCl4 |
14.常温下(I)100mL0.1mol/L的NaA溶液中的离子总物质的量为X,(Ⅱ)100mL 0.1mol/L的NaB溶液中的离子总物质的量为Y.下列推断正确的是( )
| A. | 若X>Y,则酸性:HA>HB | |
| B. | 若X=Y,则HB一定是强酸 | |
| C. | 若酸性:HA<HB,则X和Y关系不确定 | |
| D. | 若由水电离出的H+的浓度:(I)>(Ⅱ),则是X>Y |
1.H+离子与NH3分子反应生成NH4+离子,它们之间的相互作用是( )
| A. | 分子间的作用 | B. | 非极性共价键 | C. | 离子键 | D. | 配位键 |
5.从化学键的观点看,化学反应的实质是“旧键的断裂,新键的形成”,据此你认为下列变化属于化学反应的是( )
| A. | 对空气进行降温加压 | B. | 金刚石变成石墨 | ||
| C. | NaCl熔化 | D. | 碘溶于CCl4中 |
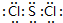 ;
;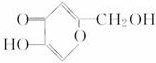 ,其所含有的官能团有(写结构简式)-$\underset{\stackrel{\;}{C}}{|}=O$、-OH、C=C、-O-.
,其所含有的官能团有(写结构简式)-$\underset{\stackrel{\;}{C}}{|}=O$、-OH、C=C、-O-.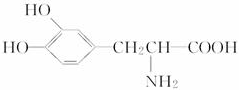 .这种药物的研制是基于获得2000年诺贝尔生理学和医学奖的研究成果.L-多巴分子中所含的官能团的名称是羟基、氨基和羧基.
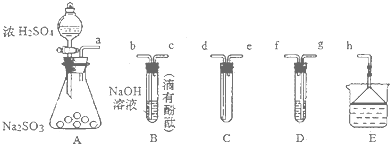
.这种药物的研制是基于获得2000年诺贝尔生理学和医学奖的研究成果.L-多巴分子中所含的官能团的名称是羟基、氨基和羧基.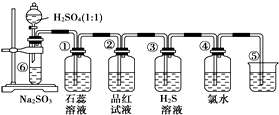 如图是实验室制备SO2并验证SO2某些性质的装置图.
如图是实验室制备SO2并验证SO2某些性质的装置图.