题目内容
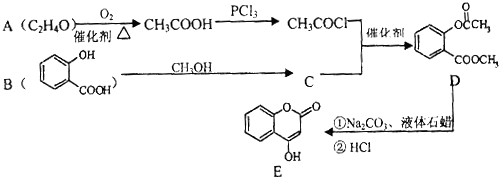
【题目】唑啉草酯H是用于麦田的具有新颖结构的苯基吡唑啉除草剂。一种合成路线如下:
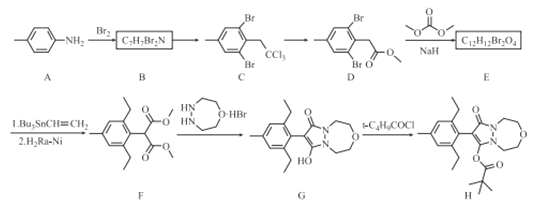
回答下列问题:
(1)A的化学名称为__________
(2)B的结构简式为__________
(3)G![]() H的反应类型为__,下列关于G、H的说法正确的是______(填选项字母)。
H的反应类型为__,下列关于G、H的说法正确的是______(填选项字母)。
A.G不含手性碳原子,H含有一个手性碳原子
B.二者均能使酸性KMnO4溶液褪色
C.二者均含有3种含氧官能团
D.二者各1mol时,最多消耗H2的物质的量不相等
(4)写出D![]() E的化学反应方程式:__________.
E的化学反应方程式:__________.
(5)同时满足下列条件的F的同分异构体Ⅰ的结构有__种(不考虑立体异构),写出一种核磁共振氢谱显示有3种不同化学环境的氢,且峰面积之比为9:1:1的Ⅰ的结构简式:_________________
①苯环上连有2个相同的叔丁基[-C(CH3)3]
②苯环上只有2个H
③1molⅠ能与2molNaHCO3反应产生无色气体
(6)结合题给信息,写出以2-甲基-1-丙烯和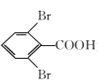 为原料(其他试剂任选)制备化合物
为原料(其他试剂任选)制备化合物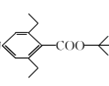 的合成路线:____________。
的合成路线:____________。
【答案】 对甲基苯胺(或对氨基甲苯) 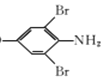 取代反应 BC
取代反应 BC 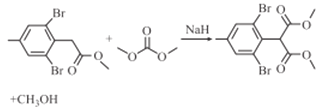 11
11 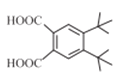 (或
(或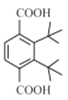 或
或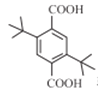 或
或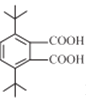 )
) 
【解析】(1)A(![]() )的化学名称为对氨基甲苯,故答案为:对氨基甲苯;
)的化学名称为对氨基甲苯,故答案为:对氨基甲苯;
(2)根据C的结构,结合A和B分子式的差别可知,B的结构简式为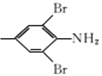 ,故答案为:
,故答案为: ;
;
(3)根据流程图,G与C4H9COCl发生取代反应生成H和氯化氢;A.G中不含手性碳原子,H中也不含手性碳原子,故A错误;B.G和H的苯环上均含有侧链烃基,能够被高锰酸钾溶液氧化,能使酸性KMnO4溶液褪色,故B正确;C.G中含有羟基、肽键和醚键3种含氧官能团,H中含有酯基、肽键和醚键3种含氧官能团,故C正确;D.肽键和酯基中的碳氧双键不能与氢气加成,1molG最多消耗4molH2,1molH4最多消耗4molH2,物质的量相等,故D错误;故选BC;故答案为:取代反应;BC;
(4)D(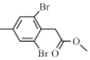 )与
)与![]() 发生取代反应生成E(
发生取代反应生成E(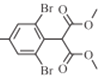 )和甲醇,反应的化学反应方程式为
)和甲醇,反应的化学反应方程式为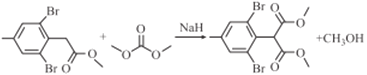 ,故答案为:
,故答案为: ;
;
(5)F为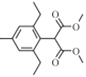 ,除变化为含有10个C,4个O。F的同分异构体Ⅰ满足:①苯环上连有2个相同的叔丁基[-C(CH3)3];②苯环上只有2个H;③1molⅠ能与2molNaHCO3反应产生无色气体,说明分子中含有2个羧基;满足条件的I是苯环上连接2个叔丁基[-C(CH3)3]和2个羧基,①2个叔丁基[-C(CH3)3]位于邻位有
,除变化为含有10个C,4个O。F的同分异构体Ⅰ满足:①苯环上连有2个相同的叔丁基[-C(CH3)3];②苯环上只有2个H;③1molⅠ能与2molNaHCO3反应产生无色气体,说明分子中含有2个羧基;满足条件的I是苯环上连接2个叔丁基[-C(CH3)3]和2个羧基,①2个叔丁基[-C(CH3)3]位于邻位有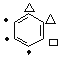 (表示叔丁基,表示羧基,表示另一个羧基可能的位置,下同)3种,
(表示叔丁基,表示羧基,表示另一个羧基可能的位置,下同)3种,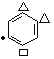 1种;②2个叔丁基[-C(CH3)3]位于间位有
1种;②2个叔丁基[-C(CH3)3]位于间位有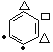 2种,
2种,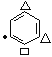 1种;③2个叔丁基[-C(CH3)3]位于对位有
1种;③2个叔丁基[-C(CH3)3]位于对位有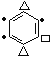 4种;共3+1+2+1+4=11种,核磁共振氢谱显示有3种不同化学环境的氢,且峰面积之比为9:1:1的Ⅰ的结构简式为
4种;共3+1+2+1+4=11种,核磁共振氢谱显示有3种不同化学环境的氢,且峰面积之比为9:1:1的Ⅰ的结构简式为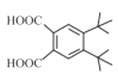 (或
(或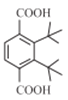 或
或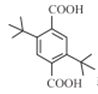 或
或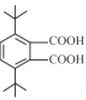 ),故答案为:
),故答案为: (或
(或 或
或 或
或 );
);
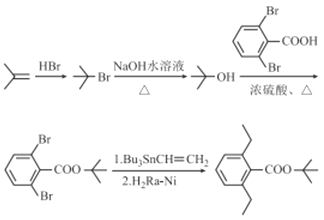
(6)以2-甲基-1-丙烯和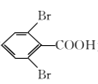 为原料制备化合物
为原料制备化合物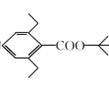 。根据流程图,需要先制备
。根据流程图,需要先制备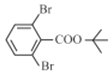 ,根据逆向推导,可以先合成
,根据逆向推导,可以先合成![]() ,可以由2-甲基-1-丙烯与溴化氢加成后水解生成,因此合成路线为
,可以由2-甲基-1-丙烯与溴化氢加成后水解生成,因此合成路线为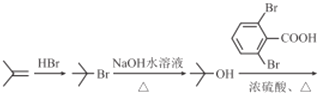
 ,故答案为:
,故答案为:
 。
。