题目内容
7.下列物质的转化在给定条件下均能通过一步反应实现的是( )| A. | NaAlO2(aq)→Al2O3→Al(OH)3 | B. | N2→NO2→HNO3 | ||
| C. | Na→Na2O2→Na2CO3 | D. | S→SO3→H2SO4 |
分析 A.偏铝酸钠溶液无法一步转化成氧化铝,氧化铝也无法一步生成氢氧化铝;
B.氮气无法一步反应生成二氧化氮;
C.钠能够与氧气加热反应生成过氧化钠,过氧化钠与二氧化碳反应生成碳酸钠;
D.硫单质无法一步反应生成三氧化硫.
解答 解:A.NaAlO2(aq)无法通过一步反应生成Al2O3,Al2O3也无法一步转化成Al(OH)3,不满足条件,故A错误;
B.NO2与水反应可以生成HNO3,但是N2无法一步反应生成NO2,故B错误;
C.Na与氧气加热反应能够直接生成Na2O2,Na2O2与二氧化碳气体也可以一步反应生成Na2CO3,所以该转化可以在给定条件下均能通过一步反应实现,满足条件,故C正确;
D.S与氧气反应生成的SO2,则无法通过一步反应实现S→SO3的转化,故D错误;
故选C.
点评 本题考查了常见元素单质及其化合物性质,题目难度中等,明确常见元素单质及其化合物的性质为解答关键,如氮气与氧气反应生成的是NO,硫单质与氧气反应生成的是二氧化硫,为易错点.

练习册系列答案
相关题目
2.NA代表阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 1.0L1.0mol•L-1的NaAlO2水溶液中含有的氧原子数数为2NA | |
| B. | 常温常压下,3.4gNH3中含N一H键数目为0.6NA | |
| C. | 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.4NA | |
| D. | 标准状况下,33.6LCCl4中含有氯原子的数目为6NA. |
3.金属钨用途广泛,主要用于制造硬质或耐高温的合金,以及灯泡的灯丝.高温下,在密闭容器中用H2还原WO3可得到金属钨,其总反应为:WO3 (s)+3H2 (g)$\stackrel{高温}{?}$W (s)+3H2O (g)
请回答下列问题:
(1)上述反应的化学平衡常数表达式为$\frac{c{\;}^{3}(H{\;}_{2}O)}{c{\;}^{3}(H{\;}_{2})}$.
(2)某温度下反应达平衡时,H2与水蒸气的体积比为2:3,则H2的平衡转化率为60%;随温度的升高,H2与水蒸气的体积比减小,则该反应为吸热反应(填“吸热”或“放热”).
(3)上述总反应过程大致分为三个阶段,各阶段主要成分与温度的关系如下表所示:
第一阶段反应的化学方程式为2WO3+H2$\frac{\underline{\;高温\;}}{\;}$W2O5+H2O;580℃时,固体物质的主要成分为W2O5、WO2;假设WO3完全转化为W,则三个阶段消耗H2物质的量之比为1:1:4.
请回答下列问题:
(1)上述反应的化学平衡常数表达式为$\frac{c{\;}^{3}(H{\;}_{2}O)}{c{\;}^{3}(H{\;}_{2})}$.
(2)某温度下反应达平衡时,H2与水蒸气的体积比为2:3,则H2的平衡转化率为60%;随温度的升高,H2与水蒸气的体积比减小,则该反应为吸热反应(填“吸热”或“放热”).
(3)上述总反应过程大致分为三个阶段,各阶段主要成分与温度的关系如下表所示:
| 温度 | 25℃~550℃~600℃~700℃ |
| 主要成份 | WO3 W2O5 WO2 W |
7.下列叙述中,不正确的是( )
| A. | 氧化还原反应的本质是电子发生转移 | |
| B. | 含化合价升高元素的反应物被氧化 | |
| C. | 得到电子的物质被氧化 | |
| D. | 2O3═3O2,不属于氧化还原反应 |
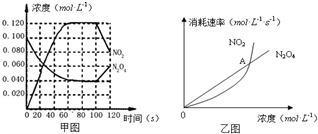 100℃时,在1L恒温恒容的密闭容器中,通入0.1mol N2O4,发生反应:N2O4(g)?2NO2(g)△H=+57.0kJ•mol-1,NO2和N2O4的浓度如图甲所示.NO2和N2O4的消耗速率与其浓度的关系如乙图所示,
100℃时,在1L恒温恒容的密闭容器中,通入0.1mol N2O4,发生反应:N2O4(g)?2NO2(g)△H=+57.0kJ•mol-1,NO2和N2O4的浓度如图甲所示.NO2和N2O4的消耗速率与其浓度的关系如乙图所示,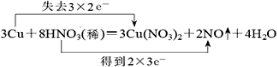 .
.