题目内容
16.按以下装置图进行实验,填写有关现象及化学方程式
(1)①撤去酒精灯后,在导管内有一段水柱形成②将E中导管口没入水面以下,③导管口E处有气泡冒出④用酒精灯微热A处试管.则证明装置气密性良好的正确操作顺序是②④③①
(2)B中浓硫酸的作用是干燥气体
(3)A中发生反应的化学方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑C中发生反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2
(4)D中发生反应的离子方程式是CO2+2OH-=CO32-+H2O
(5)如何验证收集到的E气体用带火星的木条放在集气瓶口,若木条复燃,则证明收集的气体为氧气.
分析 由图可知,A中发生2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,B中浓硫酸干燥气体,C中发生2Na2O2+2CO2=2Na2CO3+O2,D中NaOH溶液吸收氧气,最后E中排水法收集氧气,氧气具有助燃性,以此来解答.
解答 解:(1)证明装置气密性良好,操作为②将E中导管口没入水面以下、④用酒精灯微热A处试管、③导管口E处有气泡冒出、①撤去酒精灯后,在导管内有一段水柱形成,
故答案为:②④③①;
(2)B中浓硫酸的作用是干燥气体,故答案为:干燥气体;
(3)A中发生反应的化学方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,C中发生反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2,
故答案为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;2Na2O2+2CO2=2Na2CO3+O2;
(4)D中发生反应的离子方程式是CO2+2OH-=CO32-+H2O,故答案为:CO2+2OH-=CO32-+H2O;
(5)验证收集到的E气体的方法为用带火星的木条放在集气瓶口,若木条复燃,则证明收集的气体为氧气,故答案为:用带火星的木条放在集气瓶口,若木条复燃,则证明收集的气体为氧气.
点评 本题考查性质实验方案的设计,为高频考点,侧重于学生的分析与实验能力的考查,注意把握装置的作用及装置中发生的反应,难度不大,注意元素化合物知识的应用.

练习册系列答案
相关题目
6. 溴苯,无色油状液体,具有苯的气味.不溶于水,能溶于有机溶剂.实验室制取溴苯时先将铁粉和苯加入反应器,在搅拌下慢慢加入溴苯,置于70-80℃水浴中反应1h,所得粗品用水及5%氢氧化钠溶液洗涤,静置分层,蒸馏;干燥;过滤,最后经常压分馏,取156-157℃馏分而得成品.制取装置如图所示,请依据下列信息回答问题.
溴苯,无色油状液体,具有苯的气味.不溶于水,能溶于有机溶剂.实验室制取溴苯时先将铁粉和苯加入反应器,在搅拌下慢慢加入溴苯,置于70-80℃水浴中反应1h,所得粗品用水及5%氢氧化钠溶液洗涤,静置分层,蒸馏;干燥;过滤,最后经常压分馏,取156-157℃馏分而得成品.制取装置如图所示,请依据下列信息回答问题.
(1)写出制取溴苯的化学方程式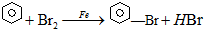 .
.
(2)仪器a的名称为三颈烧瓶,仪器c的作用是冷凝回流、导气.
(3)反应置于70-80℃水浴中而非直接加热的目的是使反应受热均匀,尽可能减少反应的挥发,防止生成的溴苯挥发.
(4)水洗后用5%氢氧化钠溶液洗涤的目的Br2+2OH-=Br-+BrO-+H2O(用离子方程式表示).
 溴苯,无色油状液体,具有苯的气味.不溶于水,能溶于有机溶剂.实验室制取溴苯时先将铁粉和苯加入反应器,在搅拌下慢慢加入溴苯,置于70-80℃水浴中反应1h,所得粗品用水及5%氢氧化钠溶液洗涤,静置分层,蒸馏;干燥;过滤,最后经常压分馏,取156-157℃馏分而得成品.制取装置如图所示,请依据下列信息回答问题.
溴苯,无色油状液体,具有苯的气味.不溶于水,能溶于有机溶剂.实验室制取溴苯时先将铁粉和苯加入反应器,在搅拌下慢慢加入溴苯,置于70-80℃水浴中反应1h,所得粗品用水及5%氢氧化钠溶液洗涤,静置分层,蒸馏;干燥;过滤,最后经常压分馏,取156-157℃馏分而得成品.制取装置如图所示,请依据下列信息回答问题.| 物质 | 溴 | 苯 | 溴苯 |
| 沸点 | 58.5℃ | 80.1℃ | 156.2℃ |
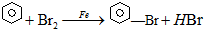 .
.(2)仪器a的名称为三颈烧瓶,仪器c的作用是冷凝回流、导气.
(3)反应置于70-80℃水浴中而非直接加热的目的是使反应受热均匀,尽可能减少反应的挥发,防止生成的溴苯挥发.
(4)水洗后用5%氢氧化钠溶液洗涤的目的Br2+2OH-=Br-+BrO-+H2O(用离子方程式表示).
7.下表为元素周期表的一部分.
(1)表中元素F的非金属性最强;元素K的金属性最强;元素Br的单质室温下呈液态(填写元素符号);
(2)表中元素⑩的原子结构示意图是 ;
;
(3)表中元素⑥⑨⑩氢化物的稳定性顺序为HF>HCl>H2S(填写化学式,下同);
(4)表中元素⑨和⑩最高价氧化物对应水化物的酸性:HClO4>H2SO4.
| 族 周期 | ⅠA | ⅡB | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 一 | ① | ||||||||
| 二 | ② | ③ | ④ | ⑤ | ⑥ | ||||
| 三 | ⑦ | ⑧ | ⑨ | ⑩ | |||||
| 四 | ⑪ | ⑫ | ⑬ | ||||||
(2)表中元素⑩的原子结构示意图是
 ;
;(3)表中元素⑥⑨⑩氢化物的稳定性顺序为HF>HCl>H2S(填写化学式,下同);
(4)表中元素⑨和⑩最高价氧化物对应水化物的酸性:HClO4>H2SO4.
4. 实验室需配制0.2000mol•L -1Na2S2O3标准溶液450mL,并利用该溶液对某浓度的NaClO溶液进行标定.
实验室需配制0.2000mol•L -1Na2S2O3标准溶液450mL,并利用该溶液对某浓度的NaClO溶液进行标定.
(1)若用Na2S2O3固体来配制标准溶液,在如图所示的仪器中,不必要用到的仪器是AB(填字母),还缺少的玻璃仪器是烧杯、玻璃棒(填仪器名称).
(2)根据计算需用天平称取Na2S2O3固体的质量是15.8g.在实验中其他操作均正确,若容量瓶用蒸馏水洗涤后未干燥,则所得溶液浓度=(填“>”“<”或“=”,下同)0.2000mol•L-1.若还未等溶液冷却就定容了,则所得溶液浓度>0.2000mol•L-1.
(3)用滴定法标定的具体方法:量取20.00mL NaClO溶液于锥形瓶中,加入适量稀盐酸和足量KI固体,用0.2000mol•L -1 Na2S2O3标准溶液滴定至终点(淀粉溶液作指示剂),四次平行实验测定的V(Na2S2O3)数据如下:
(已知:I2+2Na2S2O3═2NaI+Na2S4O6)
①NaClO溶液中加入适量稀盐酸和足量KI固体时发生反应的离子方程式为ClO-+2I-+2H+═Cl-+I2+H2O.
②NaClO溶液的物质的量浓度是0.1060 mol•L -1.
 实验室需配制0.2000mol•L -1Na2S2O3标准溶液450mL,并利用该溶液对某浓度的NaClO溶液进行标定.
实验室需配制0.2000mol•L -1Na2S2O3标准溶液450mL,并利用该溶液对某浓度的NaClO溶液进行标定.(1)若用Na2S2O3固体来配制标准溶液,在如图所示的仪器中,不必要用到的仪器是AB(填字母),还缺少的玻璃仪器是烧杯、玻璃棒(填仪器名称).
(2)根据计算需用天平称取Na2S2O3固体的质量是15.8g.在实验中其他操作均正确,若容量瓶用蒸馏水洗涤后未干燥,则所得溶液浓度=(填“>”“<”或“=”,下同)0.2000mol•L-1.若还未等溶液冷却就定容了,则所得溶液浓度>0.2000mol•L-1.
(3)用滴定法标定的具体方法:量取20.00mL NaClO溶液于锥形瓶中,加入适量稀盐酸和足量KI固体,用0.2000mol•L -1 Na2S2O3标准溶液滴定至终点(淀粉溶液作指示剂),四次平行实验测定的V(Na2S2O3)数据如下:
(已知:I2+2Na2S2O3═2NaI+Na2S4O6)
| 测定次序 | 第一次 | 第二次 | 第三次 | 第四次 |
| V(Na2S2O3)/mL | 21.90 | 18.80 | 22.10 | 22.00 |
②NaClO溶液的物质的量浓度是0.1060 mol•L -1.
1.把200mL含有CaCl2和KCl的混合溶液分成2等份,取一份加入含2a mol 碳酸钠的溶液,恰好使钙离子完全沉淀;另取一份加入含b mol硝酸银的溶液,恰好使氯离子完全沉淀.则该混合溶液中钾离子浓度为( )
| A. | 0.1(b-4a) mol•L-1 | B. | 0.1(b-2a) mol•L-1 | C. | 10(b-4a) mol•L-1 | D. | 10(b-2a) mol•L-1 |
8.综合如图判断,下列说法正确的是( )


| A. | 装置I和装置II中负极反应均是:Fe-2e-=Fe2+ | |
| B. | 装置I和装置II中盐桥中的阳离子均向右侧烧杯移动 | |
| C. | 装置I和装置II中Fe电极 的腐蚀速度为前者大于后者 | |
| D. | 放电过程中,装置I左侧烧杯和装置II右侧烧杯中溶液的PH均增大 |
5.下表是元素周期表的一部分,表中所列的字母分别代表某一种化学元素.
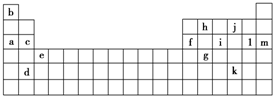
(1)上述第三周期元素中第一电离能(I1)最大的是m(用字母表示,下同),c和f的I1大小关系是c大于f.
(2)上述元素中,原子中未成对电子数最多的是i,写出该元素的电子排布式:1s22s22p63s23p3.
(3)根据下表所提供的电离能数据,回答下列问题.
①表中X可能为以上13种元素中的a元素.用元素符号表示X和j形成的化合物的化学式Na2O、Na2O2.
②Y是周期表中的ⅢA族的元素.

(1)上述第三周期元素中第一电离能(I1)最大的是m(用字母表示,下同),c和f的I1大小关系是c大于f.
(2)上述元素中,原子中未成对电子数最多的是i,写出该元素的电子排布式:1s22s22p63s23p3.
(3)根据下表所提供的电离能数据,回答下列问题.
| 锂 | X | Y | |
| I1 | 519 | 502 | 580 |
| I2 | 7296 | 4570 | 1820 |
| I3 | 11799 | 6920 | 2750 |
| I4 | 9550 | 11600 |
②Y是周期表中的ⅢA族的元素.
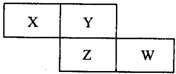 X、Y、Z、W四种短周期元素在周期表中的位置关系如图:
X、Y、Z、W四种短周期元素在周期表中的位置关系如图: :业合成该物质的化学方程式为N2+3H2$?_{催化剂}^{高温高压}$2NH3
:业合成该物质的化学方程式为N2+3H2$?_{催化剂}^{高温高压}$2NH3