题目内容
15.已知合成氨反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1,将1mol N2和3mol H2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量(忽略能量损失)( )| A. | 一定大于92.4 kJ | B. | 一定小于92.4 kJ | C. | 一定等于92.4 kJ | D. | 无法确定 |
分析 N2和H2反应生成NH3的反应为可逆反应,可逆反应不能完全进行到底,反应物的转化率不能达到100%.
解答 解:N2和H2反应生成NH3的反应为可逆反应,反应为:N2+3H2 2NH3,可逆反应不能完全进行到底,反应物的转化率不能达到100%,此温度下的1molN2和3molH2放在一密闭容器中,不能生成2molNH3,则反应放出的热量小于92.4kJ,
2NH3,可逆反应不能完全进行到底,反应物的转化率不能达到100%,此温度下的1molN2和3molH2放在一密闭容器中,不能生成2molNH3,则反应放出的热量小于92.4kJ,
故选B.
点评 本题考查化学反应的可逆性,题目难度不大,注意把握可逆反应的特征,应不能完全进行到底,反应物的转化率不能达到100%.

练习册系列答案
相关题目
5.下列说法正确的是( )
| A. | 液态 HCl、固体NaCl 均不导电,所以 HCl、NaCl 均是非电解质 | |
| B. | NH3、CO2的水溶液均导电,所以 NH3、CO2 均是电解质 | |
| C. | 铜、石墨均导电,所以它们是电解质 | |
| D. | 蔗糖、酒精在水溶液或熔化时均不导电,所以它们是非电解质 |
6.下列各组物质按酸、碱、盐分类顺序排列正确的是( )
| A. | 盐酸、纯碱、石膏 | B. | 硫酸、烧碱、绿矾 | ||
| C. | 碳酸、乙醇、醋酸钠 | D. | 磷酸、熟石灰、可性钾 |
3.在硫化氢的水溶液中,存在以下平衡:H2S═HS-H+、HS-═H++S2-,若使溶液的pH减小,则c(S2-)( )
| A. | 增大 | B. | 减小 | ||
| C. | 不变 | D. | 可能增大也可能减小 |
10.澄清透明的溶液中能大量共存的是( )
| A. | Cu2+、C1-、SO42-、K+ | B. | K+、OH-、CO32-、Fe2+ | ||
| C. | Ca2+、OH-、C1-、Na+ | D. | Ag+、NO3-、Cl-、K+ |
20.在一密闭容器中,反应aA(g)?bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度变为原来的60%,则( )
| A. | 平衡向逆反应方向移动了 | B. | 物质A的转化率增大了 | ||
| C. | 物质B的质量分数减小了 | D. | a>b |
7.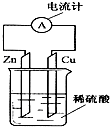 如图所示,把锌片和铜片用导线相连后插入稀硫酸溶液中构成原电池.下列叙述正确的是( )
如图所示,把锌片和铜片用导线相连后插入稀硫酸溶液中构成原电池.下列叙述正确的是( )
 如图所示,把锌片和铜片用导线相连后插入稀硫酸溶液中构成原电池.下列叙述正确的是( )
如图所示,把锌片和铜片用导线相连后插入稀硫酸溶液中构成原电池.下列叙述正确的是( )| A. | 电流从铜片经导线流向锌片 | B. | 该装置将电能转变为化学能 | ||
| C. | 一段时间后,铜片质量减轻 | D. | 锌片发生还原反应 |