题目内容
13.下列说法不正确的是( )| A. | 常温下,在0.1mol/L氨水中,加入少量NH4Cl晶体,溶液的pH减小 | |
| B. | 反应2Mg(s)+CO2(g)=C(s)+2MgO(s)能自发进行,则该反应的△H<0 | |
| C. |  滴定达终点时,图滴定管的正确读数为23.65 mL 滴定达终点时,图滴定管的正确读数为23.65 mL | |
| D. | 温度一定时,水的离子积常数Kw不随外加酸(碱)浓度的改变而改变 |
分析 A、从影响NH3•H2O?NH4++OH-的平衡移动角度考虑;
B、反应能否自发进行,决定于有△H-T△S;
C、滴定管的0刻度在上方;
D、水的离子积常数只受温度影响.
解答 解:A、氨水中存在NH3•H2O?NH4++OH-,加入NH4Cl晶体时,NH4+的浓度增大,平衡逆向移动,OH-浓度减小,氢离子浓度就会增大,pH就会减小,故A正确;
B、反应物中有气体,生成物中没有气体,故△S<0,若要使反应自发进行,△H-T△S<0,则△H必须小于0,故B正确;
C、滴定管的0刻度在上方,图滴定管的正确读数为22.65 mL,故C错误;
D、水的离子积常数只受温度影响,与外加酸碱无关,故D正确.
故选C.
点评 本题考查了弱电解质的电离平衡移动、反应自发进行的条件、滴定管的读数、水的离子积常数只受温度影响,题目难度不大,注意滴定管与量筒的0刻度位置.

练习册系列答案
相关题目
3.下列说法中正确的是( )
| A. | 物质发生化学反应都伴随着能量变化 | |
| B. | 伴有能量变化的物质变化都是化学变化 | |
| C. | 在一个确定的化学反应关系中,反应物的总能量与生成物的总能量可以相同 | |
| D. | 在一个确定的化学反应关系中,反应物的总能量总是高于生成物的总能量 |
4.某有机物的结构简式如图所示,关于该有机物的说法不正确的是( )
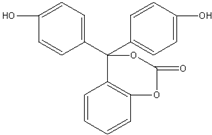

| A. | 该有机物的化学式为C20H14O5 | |
| B. | 该有机物分子中的三个苯环不可能共平面 | |
| C. | 该有机物可发生加成、取代、氧化、消去等反应 | |
| D. | 1mol该有机物与足量NaOH 溶液充分反应,消耗NaOH的物质的量为5 mol |
1.用水稀释0.1mol L-1的醋酸溶液,其中随水的增加而增大的有( )
①H+的物质的量,②c(H+),③c(OH-),④$\frac{c({H}^{+})}{c(HAc)}$,⑤$\frac{c(HAc)}{c(A{c}^{-})}$.
①H+的物质的量,②c(H+),③c(OH-),④$\frac{c({H}^{+})}{c(HAc)}$,⑤$\frac{c(HAc)}{c(A{c}^{-})}$.
| A. | ①③④ | B. | ①③⑤ | C. | ②④ | D. | ③④ |
18.醋酸钡[(CH3COO)2Ba•H2O]是一种媒染剂,下列是有关0.1mol/L醋酸钡溶液中粒子浓度的比较,其中错误的是( )
| A. | c(H+)=c(OH-)-c(CH3COOH) | B. | c(H+)+2c(Ba2+)=c(CH3COO-)+c(OH-) | ||
| C. | c(Ba2+)>c(CH3COO-)>c(OH-)>c(H+) | D. | 2c(Ba2+)=c(CH3COO-)+c(CH3COOH) |
2.基态铬原子的电子排布式是( )
| A. | 1S22S22p63S23p64S14p5 | B. | 1S22S22p63S23d54S1 | ||
| C. | 1S22S22p63S23p63d6 | D. | 1S22S22p63S23p64S23d4 |
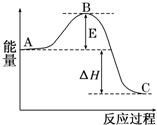 2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1molSO3(g)的△H=-99kJ/mol.
2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1molSO3(g)的△H=-99kJ/mol.