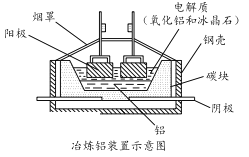
题目内容
【题目】现用Na2SO4固体来配制480mL0.2mol·L-1的Na2SO4溶液。可供选择的仪器如图:
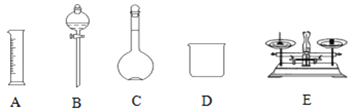
(1)如图所示的仪器中配制溶液不需要的是__ (填选项),配制上述溶液还需用到的玻璃仪器是___、__ (填仪器名称)。
(2)使用容量瓶之前必须进行的操作是___。(填选项)
A.检查气密性 B.检查是否漏水 C.烘干
(3)经计算,需Na2SO4的质量为___g。
(4)你选用的容量瓶规格为___mL。
(5)配制溶液时,一般可分为以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容
其操作顺序:②→__→__→__→__→__→__(填序号)。___
(6)在配制过程中,其他操作都准确,定容时俯视刻度线会使所配溶液浓度__(填“偏高”、“偏低”或“无影响”)。
【答案】B 胶头滴管 玻璃棒 B 14.2 500 ①③⑤⑥⑦④ 偏高
【解析】
(1)根据配制一定物质的量浓度溶液的操作步骤选取实验仪器;
(2)容量瓶带有瓶塞,为防止使用过程中漏水,使用前应检查是否漏液;
(3)依据m=cVM计算;
(4)根据实验室常见容量瓶的规格选择;
(5)根据配制一定物质的量浓度溶液的操作步骤排序;
(6)定容时俯视刻度线,会导致溶液的体积偏小,据此分析判断。
(1)配制一定物质的量浓度的溶液的步骤有称量、溶解、移液、洗涤、定容、摇匀等操作,一般用托盘天平称取硫酸钠,在烧杯中溶解,冷却后转移到500mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以需要的仪器有托盘天平、玻璃棒、量筒、胶头滴管、小烧杯、500mL容量瓶,所以用不到的仪器有分液漏斗,还缺少的仪器:胶头滴管、玻璃棒,故答案为:B;胶头滴管;玻璃棒;
(2)容量瓶带有瓶塞,为防止使用过程中漏水,使用前应检查是否漏液,故答案为:B;
(3)实验室没有480mL的容量瓶,应该选用500 mL的容量瓶配制,Na2SO4的质量为0.5L×0.2mol/L×142g/mol=14.2g,故答案为:14.2;
(4)实验室没有480mL的容量瓶,应该选用500 mL的容量瓶配制,故答案为:500;
(5)配制一定物质的量浓度的溶液的步骤有计算、称量、溶解、冷却、移液、洗涤、定容、摇匀等操作,所以正确的操作顺序为②①③⑤⑥⑦④,故答案为:①③⑤⑥⑦④;
(6)在配制过程中,其他操作都准确,定容时俯视刻度线,导致溶液的体积偏小,会使所配溶液浓度偏高,故答案为:偏高。

【题目】硫酸铜是一种应用极其广泛的化工原料;以下是某工厂用含铁废铜为原料生产胆矾(CuSO45H2O)和副产物石膏(CaSO42H2O)的生产流程示意图:
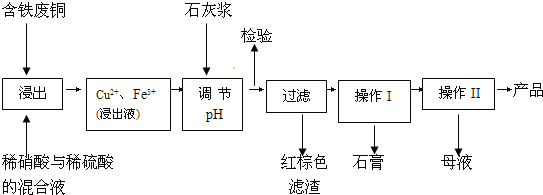
胆矾和石膏在不同温度下的溶解度(g/100g水)见表。
温度(℃) | 20 | 40 | 60 | 80 | 100 |
石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
胆矾 | 32 | 44.6 | 61.8 | 83.8 | 114 |
请回答下列问题:
(1)红棕色滤渣的主要成分是___;
(2)写出浸出过程中生成硫酸铜的离子方程式___;
(3)操作I包括蒸发浓缩、__等操作,温度应该控制在__℃左右;
(4)从溶液中分离出硫酸铜晶体的操作Ⅱ应为__、___、洗涤、干燥;晶体用无水乙醇作洗涤液而不用蒸馏水的原因是__;干燥时采用晾干,不用加热烘干的原因是___。
(5)取样检验是为了确认Fe3+是否除净。有同学设计了以下两种方案,在实验室分别对所取样品按下列方案进行操作:
方案一:取样于试管→滴加KSCN溶液; 方案二:纸层析→喷KSCN溶液;
①你认为上述两种方案设计更合理的是__;
②指出你认为不合理方案存在的问题是__。
【题目】金属镍在电池和电镀等工业上具有广泛的用途,可镍也具有很强的毒性,若不进行回收处理,将对环境造成很大的影响,以下是以电镀废渣为原料获得NiSO46H2O的过程,已知,废渣中除含金属镍外,主要含有:Cu、Zn、Fe、Mg等元素的化合物。
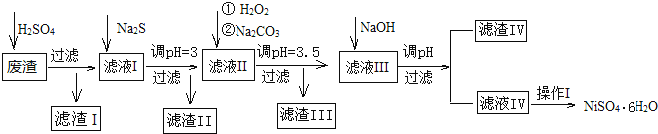
部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH见表.
沉淀物 | Fe(OH)3 | Fe(OH)2 | CuS | ZnS | FeS | NiS | Al(OH)3 | Mg(OH)2 | Ni(OH)2 |
pH | 3.2 | 9.7 | ≥-0.42 | ≥2.5 | ≥7 | ≥7.5 | ≥5 | ≥8 | ≥8.5 |
(1)往废渣中加H2SO4酸浸,提高酸浸效率的方法有__(至少写出2点)。
(2)加Na2S同时调溶液的pH为3,目的是除去铜、锌等杂质,则往滤液Ⅱ中加入H2O2的反应的离子方程式为___。
(3)操作Ⅰ包括以下过程:__、__、过滤、洗涤、干燥.该洗涤过程不能用水洗涤,应该用__洗涤,目的是___。干燥有低温干燥和高温干燥,能否用高温干燥___,理由是____。
(4)滤液Ⅲ中加入NaOH溶液的目的是调节溶液的pH为8以除去Al3+以及少量的Mg2+,若向含有Mg2+、Al3+的溶液中滴加NaOH溶液,常温下当两种沉淀共存且溶液的pH=8时,c(Mg2+):c(Al3+)=__。{已知:25℃时,Ksp[Mg(OH)2]=5.0×10-14;Ksp[Al(OH)3]=2.0×10-33}。