题目内容
20.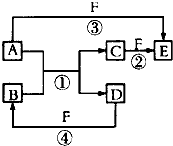 A、B、C、D、E、F是中学中常见的物质,其转化关系如图所示(反应条件未标出),已知反应①是置换反应.
A、B、C、D、E、F是中学中常见的物质,其转化关系如图所示(反应条件未标出),已知反应①是置换反应.请回答下列问题:
(1)若B是黄绿色气体,C、F是空气的主要成分,A、D相遇有白烟生成,写出A的电子式
 ,反应③的化学方程式为4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
,反应③的化学方程式为4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.(2)若A、D、F都是非金属单质,A、D所含元素同主族,A、F 所含元素同周期,则B所属晶体结构类型是原子晶体,其一个重要的用途是光导纤维、石英钟表、石英玻璃等.
(3)若A是常见的金属单质,D、F是气态单质,反应①②在水溶液中进行,则工业上冶炼金属A的反应原理是(用化学方程式表示)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
(4)若A、D是常见单质,且所含元素的原子序数A是D的2倍,原子最外层电子数D是A的2倍,反应③④中都有红棕色气体生成.则反应①的化学方程式为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.
分析 (1)若B是黄绿色气体应为Cl2,C、F是空气的主要成分,结合转化关系F为O2,由于氧的氧化性较氯气稍强,故氯气置换出的应该是氮气,C为N2,C+F→E,为N2+O2$\frac{\underline{\;放电\;}}{\;}$2NO;A、D相遇有白烟生成,判断A为NH3,D为HCl;
(2)反应①是置换反应,而且涉及的单质都是非金属,所以可以考虑氧族里氧气置换出硫的反应,卤素单质之间的置换(氧化性较强的单质置换出氧化性较弱的单质);碳族里碳置换出硅的反应.再结合与F的反应可以推断出B应该是二氧化硅,原子晶体;
(3)金属置换出气体很容易就想到活泼金属置换出氢气,再结合能与F连续反应,可以推断出是铁和盐酸的反应;反应②的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-
(4)由最外层电子数的关系可知,A的电子数较少,还原性较强的物质置换出还原性较弱的物质,很容易想到最外层两个电子的镁与碳的置换反应.
解答 解:(1)若B是黄绿色气体应为Cl2,C、F是空气的主要成分,结合转化关系F为O2,由于氧的氧化性较氯气稍强,故氯气置换出的应该是氮气,C为N2,C+F→E,为N2+O2$\frac{\underline{\;放电\;}}{\;}$2NO;A、D相遇有白烟生成,所以发生反应为NH3+HCl=NH4Cl,判断A为NH3,A的电子式为 ,D为HCl;该白烟的化学式为:NH4Cl;反应③是氨气催化氧化为一氧化氮的反应,化学方程式:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,
,D为HCl;该白烟的化学式为:NH4Cl;反应③是氨气催化氧化为一氧化氮的反应,化学方程式:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,
故答案为: ;4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;
;4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;
(2)若A、D、F都是非金属单质,A、D所含元素同主族,A、F所含元素同周期,反应A+B→C+D是非金属间的置换反应,可以分析第ⅣA、ⅥA、ⅤⅡA 主族元素单质间的置换反应,结合转化关系中 F的反应,只有2C+SiO2=Si+2CO 符合,所以A为C,B为 SiO2; 原子晶体(2分);任选一种(2分).二氧化硅属于原子晶体,主要用途为:光导纤维、石英钟表、石英玻璃等,
故答案为:原子晶体;光导纤维、石英钟表、石英玻璃等;
(3)若A是常见的金属单质,D、F是气态单质,反应①②在水溶液中进行,结合能与F连续反应,说明存在变价,可以推断出是铁和盐酸的反应,工业上冶炼金属Fe的反应原理为一氧化碳还原氧化铁,反应的化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,
故答案为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(4)若A、D是常见单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,结合原子结构可知是镁置换碳的反应,反应③④中都有红棕色气体生成,说明生成了NO2,则F为浓硝酸,反应①的化学方程式为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C,
故答案为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.
点评 本题考查了无机物质转化关系和性质的综合推断,常见置换反应的特征和类型,主要考查氯单质及其化合物、氮及其化合物性质的转化关系和应用,特征置换反应和特征现象的应用是解题关键.

| A. | SO32-→SO2 | B. | HCl→Cl2 | C. | Na→Na+ | D. | CO2→CO |
| A. | 由非金属元素形成的化合物一定不是离子化合物 | |
| B. | 含有金属元素的化合物一定是离子化合物 | |
| C. | 活泼金属与活泼非金属化合时,能形成离子键 | |
| D. | 第IA族和VIIA族原子化合时,一定生成离子键 |
| A. | pH=2的HA溶液与pH=12的MOH溶液等体积混合后pH<7,则HA为弱酸 | |
| B. | pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH)<c(Na2CO3)<c(CH3COONa) | |
| C. | 物质的量浓度均为0.2mol•L-1CH3COOH和CH3COONa溶液等体积混合:2c(Na+)=c(CH3COO-)+c(CH3COOH)=0.2mol•L-1 | |
| D. | 0.1mol•L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-) |
| A. | 原混合气体中 O2 和CH4 体积比为2:1 | |
| B. | 原混合气体中 O2 和CH4 体积比为1:1 | |
| C. | 残留固体中只有Na2CO3 | |
| D. | 残留固体中只有Na2CO3 和NaOH |
| A. | CH2Cl2有 和 和 两种结构 两种结构 | |
| B. | 烯烃跟氢气起加成反应产物是2,2,3,4-四甲基戊烷,则这样的烯烃有3种 | |
| C. | 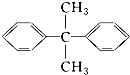 的一氯代物有5种 的一氯代物有5种 | |
| D. | 1 mol某烷烃完全燃烧消耗11 mol O2,则其主链上含有5个碳原子的同分异构体(不考虑空间异构)有6种 |
| A. | NF既是氧化剂,又还原剂 | |
| B. | 还原剂与氧化剂的物质的量之比为1:2 | |
| C. | 若生成2molHNO3,则转移2mol电子 | |
| D. | NF3中氢元素的化合价为+3 |
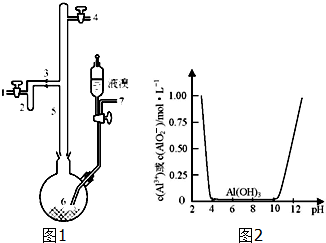 利用废铝箔(主要成分为Al、少量的Fe、Si等)既可制取有机合成催化剂AlBr3又可制取净水剂硫酸铝晶体.
利用废铝箔(主要成分为Al、少量的Fe、Si等)既可制取有机合成催化剂AlBr3又可制取净水剂硫酸铝晶体.