题目内容
15.常温下,下列溶液中有关物质的量浓度关系不正确的是( )| A. | pH=2的HA溶液与pH=12的MOH溶液等体积混合后pH<7,则HA为弱酸 | |
| B. | pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH)<c(Na2CO3)<c(CH3COONa) | |
| C. | 物质的量浓度均为0.2mol•L-1CH3COOH和CH3COONa溶液等体积混合:2c(Na+)=c(CH3COO-)+c(CH3COOH)=0.2mol•L-1 | |
| D. | 0.1mol•L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-) |
分析 A.弱酸在溶液中部分电离,则HA的浓度大于MOH,混合液中AH过量,溶液显示酸性;
B.氢氧化钠为强电解质,pH相等时其浓度最小,碳酸的酸性小于醋酸的酸性,则pH相等时c(Na2CO3)<c(CH3COONa);
C.根据混合液中的物料守恒分析;
D.NaHA溶液的pH=4,说明的电离程度大于其水解程度,则c(A2-)>c(H2A).
解答 解:A.pH=2的HA溶液与pH=12的MOH溶液等体积混合后,若HA为强酸,则反应后的溶液呈中性,溶液的pH=7,而二者反应后的溶液的pH<7,则说明HA为弱酸,混合液中HA过量,故A正确;
B.pH相等的CH3COONa、NaOH和Na2CO3三种溶液,NaOH为强碱,则其浓度最小;碳酸的酸性小于醋酸的酸性,则pH相等时c(Na2CO3)<c(CH3COONa),所以pH相等时各物质的浓度大小为:c(NaOH)<c(Na2CO3)<c(CH3COONa),故B正确;
C.物质的量浓度均为0.2mol•L-1CH3COOH和CH3COONa溶液等体积混合,根据物料守恒可得:2c(Na+)=c(CH3COO-)+c(CH3COOH)=0.2mol•L-1,故C正确;
D.0.1mol•L-1的NaHA溶液,其pH=4,说明的电离程度大于其水解程度,则c(A2-)>c(H2A),正确的离子浓度大小为:c(HA-)>c(H+)>c(A2-)>c(H2A),故D错误;
故选D.
点评 本题考查了离子浓度大小比较,题目难度中等,明确盐的水解原理及其影响为解答关键,注意掌握电荷守恒、物料守恒、盐的水解原理等知识在判断离子浓度大小中的应用方法.

练习册系列答案
 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
10.下列说法正确的是( )
| A. | “春蚕到死丝方尽,蜡烛成灰泪始干”中的“丝”、“泪”分别是纤维素和油脂 | |
| B. | 乙醇、金属钠和乙酸分别属于非电解质、非电解质和弱电解质 | |
| C. | Na2O2、Al2O3、C4H10分别属于碱性氧化物、两性氧化物和离子化合物 | |
| D. | 煤的气化、石油的分馏分别是化学变化、物理变化 |
 .若烃A能使溴水褪色,在催化剂作用下,与H2加成反应后生成2,2-二甲基丁烷,则烃A的名称是3,3-二甲基-1-丁烯,结构简式是(CH3)3C-CH=CH2.比烃A少两个碳原子且能使溴水褪色的A的同系物有3种同分异构体.
.若烃A能使溴水褪色,在催化剂作用下,与H2加成反应后生成2,2-二甲基丁烷,则烃A的名称是3,3-二甲基-1-丁烯,结构简式是(CH3)3C-CH=CH2.比烃A少两个碳原子且能使溴水褪色的A的同系物有3种同分异构体.
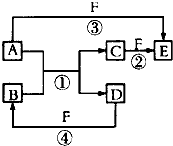 A、B、C、D、E、F是中学中常见的物质,其转化关系如图所示(反应条件未标出),已知反应①是置换反应.
A、B、C、D、E、F是中学中常见的物质,其转化关系如图所示(反应条件未标出),已知反应①是置换反应. ,反应③的化学方程式为4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
,反应③的化学方程式为4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
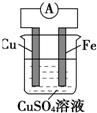 如图所示,
如图所示,