题目内容
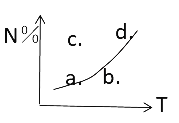
【题目】如图曲线表示其他条件一定时,反应2M(g)+N(g)![]() 2R(g) ΔH<0,达到平衡时N的体积分数与温度的关系曲线,图中标有a、b、c、d四点,其中v正<v逆的点是
2R(g) ΔH<0,达到平衡时N的体积分数与温度的关系曲线,图中标有a、b、c、d四点,其中v正<v逆的点是
A. a点 B. b点
C. c点 D. d点
【答案】B
【解析】
在曲线上,当温度一定时,N的体积分数也一定,故曲线上任意一点都表示达到平衡状态,而曲线外的任意一点都表示未达平衡状态。在曲线下方的任意一点,要想达到同温度下的平衡状态,即向上引垂直线到曲线上的一点,这样N的体积分数要增大,平衡向左移动,在曲线上方的任意一点,要想达到同温度下的平衡状态,即向下引垂直线到曲线上的一点,这样N的体积分数要减小,平衡向右移动,据此解答。
A、a点在曲线上,处于平衡状态,v正=v逆,故A错误;
B、b点在曲线下方,未达到平衡状态,要想达到同温度下的平衡状态,即由b点向上引垂直线到曲线上的一点,这样N的体积分数要增大,平衡向左移动,故v正<v逆,故B正确;
C、c点在曲线上方,未达到平衡状态,要想达到同温度下的平衡状态,即由c点向下引垂直线到曲线上的一点,这样N的体积分数要减小,平衡向右移动,故v正>v逆,故C错误;
D、d点在曲线上,处于平衡状态,v正=v逆,故D错误。
答案选B。

 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案【题目】对利用甲烷消除NO2污染进行研究,CH4+2NO2 ![]() N2+CO2+2H2O。在1L密闭容器中,控制不同温度,分别加入0.50molCH4和1.2molNO2,测得n(CH4)随时间变化的有关实验数据见下表。
N2+CO2+2H2O。在1L密闭容器中,控制不同温度,分别加入0.50molCH4和1.2molNO2,测得n(CH4)随时间变化的有关实验数据见下表。
组别 | 温度 | 时间/min n/mol | 0 | 10 | 20 | 40 | 50 |
① | T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
② | T2 | n(CH4) | 0.50 | 0.30 | 0.18 | … | 0.15 |
下列说法正确的是
A. 组别①中,0~20min内,NO2的降解速率为0.0125 mol·L-1·min-1
B. 由实验数据可知实验控制的温度T12
C. 40min时,表格中T2应填的数据为0.18
D. 0~10min内,CH4的降解速率①>②
【题目】实现 “节能减排” 和“低碳经济”是化学工作者研究的重要课题。有一种用CO2生产甲醇燃料的方法:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
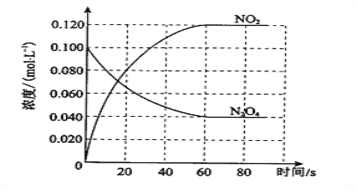
(1)CO2和H2充入一定体积的密闭容器中,两种温度下CH3OH的物质的量随时间的变化见图1。曲线I、Ⅱ对应的平衡常数大小关系为KⅠ____KⅡ(填“>”、“<”或“=”)。

(2)某实验中将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图2曲线(甲)所示。
①a点正反应速率_________逆反应速率(填“>”、“<”或“=”);
0-10min内v(CH3OH) =__________mol·L-1·min-1。
②若仅改变某一条件再进行实验,测得H2的物质的量随时间变化如图中虚线(乙)所示。曲线(乙)对应改变的实验条件可以是______填序号)。
A.加催化剂 B.增大压强
C.升高温度 D.增大CO2浓度
(3)830 ℃,反应的平衡常数K=1。在2L恒容反应器中发生上述反应,按下表中A、B、C、D四组的物质的量投入反应混合物,其中向正反应方向进行的有_____(填序号)。
物质 | A | B | C | D |
n(CO2) | 3 | 1 | 3 | 1 |
n(H2) | 2 | 2 | 4 | 0 |
n(CH3OH) | 1 | 2 | 3 | 0.5 |
n(H2O) | 0 | 2 | 3 | 2 |
(4)研究发现,在相同条件下还发生另一个平行反应CO2(g)+H2(g)![]() CO(g)+H2O(g)。CO2与H2用量相同,使用不同的催化剂时,产物中CO与CH3OH比例有较大差异,其原因是__________________________ 。
CO(g)+H2O(g)。CO2与H2用量相同,使用不同的催化剂时,产物中CO与CH3OH比例有较大差异,其原因是__________________________ 。