题目内容
13.研制和开发不含碳并可工业生产的清洁能源,一直是科学家不懈追求的目标.目前液氨被人们视为一种潜在的清洁燃料.液氨燃烧的化学反应方程式为:4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O.和氢燃料相比有关数据见下表,据此判断正确的是( )| 燃料 | 沸点/℃ | 燃烧热/(kJ•mol-1) | 相对分子质量/(g•mol-1) | 液态密度/(g•cm-3) |
| 氢 | -252.60 | 238.40 | 2.02 | 0.07 |
| 氨 | -33.50 | 317.10 | 17.03 | 0.61 |
②氨泄漏到空气中比氢气更易发生爆炸
③等质量的氨和氢分别燃烧,氨放出的热量多
④氨的液化比氢容易得多.
| A. | ①③ | B. | ②③ | C. | ①④ | D. | ②④ |
分析 ①依据氨气、氢气燃烧产物判断;
②氨气与氧气反应需要在催化剂条件下进行;
③依据燃烧热和相对分子质量求出等质量的氨和氢放出的热量并进行比较;
④氨气的熔沸点高于氢气.
解答 解:①NH3燃烧生成N2和H2O,H2为燃烧生成H2O,以NH3和H2为燃料,反应的产物只有N2和H2O,不会生成二氧化碳,所以可以减缓温室效应,故正确;
②氨气在空气中难以与氧气反应,并且有强烈刺激性,当不慎泄漏时,不易发生爆炸,故错误;
③设氨气和氢气的质量为a,氨气燃烧放出的热量=$\frac{a}{17}$×317.1≈18.7akJ,氢气放出的热量=$\frac{a}{2}$×238.4≈118.02akJ,119.2kJ>18.7akJ,所以等质量的氨和氢分别燃烧,氢放出的热量多,故错误;
④氨气的熔沸点高于氢气,所以氨气易液化,故正确;
故选:C.
点评 本题考查了氨气的性质,熟悉氨气的性质、清楚图中数据的含义是解题关键,题目难度不大.

练习册系列答案
相关题目
3.下列离子方程式正确的是( )
| A. | Ca(HCO3)2溶液与过量Ca(OH)2溶液反应:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| B. | 用惰性电极电解MgCl2溶液:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$H2↑+Cl2↑+2OH- | |
| C. | 氯气通入水中:C12+H2O═2H++C1-+C1O- | |
| D. | 亚硫酸钡与稀硝酸反应:BaSO3+2H+═Ba2++SO2↑+H2O |
4.具有下列结构的原子一定属于第二主族的是( )
| A. | 最外层电子数与次外层电子数相等的原子 | |
| B. | M层电子数为K层电子数一半的原子 | |
| C. | 最外层有2个电子的原子 | |
| D. | M层电子数等于其内层电子数之和$\frac{1}{5}$的原子 |
1.下列有关反应中的能量变化图象的判断错误的是( )
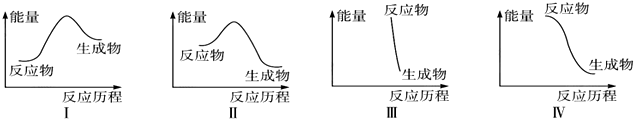

| A. | Ⅰ可表示放热反应 | B. | Ⅱ可表示放热反应 | ||
| C. | Ⅲ可表示爆炸反应 | D. | Ⅳ可表示醋酸和碱的中和反应 |
8.某物质结构如图.下列有关该物质的说法正确的是( )
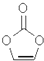

| A. | 分子式为C3H4O3 | B. | 分子中含8个σ键 | ||
| C. | 分子中只有极性键 | D. | 8.6g该物质完全燃烧得到6.72LCO2 |
18.一定质量的某有机物与足量的钠反应生成V1L气体.等量的该有机物与过量的NaHCO3反应,生成相同状况下的气体V2L.若V1>V2.该有机物可能是下列中的( )
| A. | HOOC-COOH | B. | HO(CH2)2COOH | C. | CH2OHCHOHCOOH | D. | (CH3)3CCOOH |
5.等体积混合0.1mol•L-1的盐酸和0.06mol•L-1的Ba(OH )2溶液,不考虑体积效应,即认为混合溶液的体积等于进行混合的两溶液体积之和,溶液的pH值等于( )
| A. | 2.0 | B. | 12.3 | C. | 1.7 | D. | 12.0 |
2.与乙烯所含碳、氢元素的百分含量相同,但与乙烯既不是同系物又不是同分异构体的是( )
| A. |  | B. | 乙烷 | C. | 甲烷 | D. | CH3CH=CH2 |
3.标准状况下,11.2L的下列混合气体完全燃烧后,测得水的质量为22.5g,二氧化碳的质量为44g.该混合气体是( )
| A. | 甲烷和乙烷 | B. | 乙烯和乙烷 | C. | 乙烷和丙烯 | D. | 甲烷和丙烷 |