题目内容
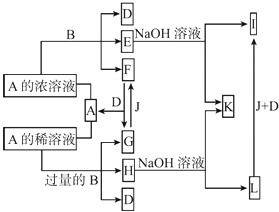
【题目】向20mL某浓度的AlCl3溶液中滴加2mol/L的NaOH溶液时,所得的沉淀质量与加入NaOH溶液的体积之间的关系如图所示:

(1)分别用离子方程式表示图中OA段、AB段的反应原理_________________________、_____________________________.
(2)最大沉淀质量为_____g
(3)所用AlCl3溶液的物质的量浓度是______________
(4)当所得沉淀量为0.39g时,用去NaOH溶液的体积是_____mL或_____mL。
【答案】 图中OA段:Al3++3OH-=Al(OH)3↓ AB段:Al(OH)3+OH-=AlO2-+2H2O 0.78 g 0.5mol/L 7.5 mL 17.5 mL。
【解析】(1)开始AlCl3与NaOH反应Al3++3OH-= Al(OH)3↓,生成Al(OH)3沉淀,NaOH量逐渐增多,Al(OH)3量逐渐增大,到A点时氢氧化钠将AlCl3恰好完全沉淀时,Al(OH)3沉淀达到最大量,故图中OA段离子反应为:Al3++3OH-=Al(OH)3↓;Al(OH)3沉淀达到最大量后,再加NaOH,发生Al(OH)3+OH-=AlO2-+2H2O,沉淀量又逐渐减少,到B点时Al(OH)3与NaOH恰好完全反应生成NaAlO2,沉淀完全溶解消失,故图中AB段离子反应为:Al(OH)3+OH-=AlO2-+2H2O;(2)由于A→B消耗的氢氧化钠溶液体积为5mL,消耗NaOH为0.005L×2mol/L=0.01 mol,根据方程式可知n[Al(OH)3]=0.01mol,氢氧化铝的质量=0.01mol×78g/mol=0.78g;(3)根据铝原子守恒,则n(AlCl3)=n[Al(OH)3]=0.01mol,故氯化铝的物质的量浓度=![]() =0.5mol/L;(5)0.39 g Al(OH)3的物质的量=
=0.5mol/L;(5)0.39 g Al(OH)3的物质的量=![]() =0.005mol。当NaOH溶液不足时,生成0.39 g Al(OH)3所需NaOH的物质的量为0.005mol×3=0.015 mol,需要NaOH溶液的体积=
=0.005mol。当NaOH溶液不足时,生成0.39 g Al(OH)3所需NaOH的物质的量为0.005mol×3=0.015 mol,需要NaOH溶液的体积=![]() =0.0075L=7.5mL;当NaOH溶液过量时,还剩余0.39 g Al(OH)3,剩余0.39 g Al(OH)3溶解可以消耗0.005molNaOH,故共消耗NaOH的物质的量=0.02L×2mol/L-0.005mol=0.035 mol,需要NaOH溶液的体积=
=0.0075L=7.5mL;当NaOH溶液过量时,还剩余0.39 g Al(OH)3,剩余0.39 g Al(OH)3溶解可以消耗0.005molNaOH,故共消耗NaOH的物质的量=0.02L×2mol/L-0.005mol=0.035 mol,需要NaOH溶液的体积=![]() =0.0175L=17.5mL,故答案为:7.5 mL或17.5 mL。
=0.0175L=17.5mL,故答案为:7.5 mL或17.5 mL。

【题目】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题;(回答问题时,均需使用元素的真实元素符号,不得使用数字编号)
族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | Ⅷ |
1 | ① | |||||||
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ |
(1)②、⑤、⑥的离子半径由大到小的顺序为
(2)写出由①、②两元称组成,且①的质量分数最高的分子的电子式 ,
写出该化合物跟⑧的单质发生置换反应的化学方程式 .
(3)元素⑥的最高价氧化物可和元素⑤的氢氧化物水溶液发生反应,写出反应的离子方程式
(4)元素③有多种氧化物,其中甲的相对分子质量最小;元素④有多种单质,其中乙的相对分子质量最小.在一定条件下,将2L 甲气体与1.5L 乙气体均匀混合,若该混合气体被足量NaOH 溶液完全吸收(没有气体残留).所生成的含氧酸盐的化学式是 .
【题目】下列物质分类的正确组合是( )
碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
A | Cu2(OH)2CO3 | H2SO4 | NaHCO3 | SiO2 | CO2 |
B | NaOH | HCl | NaCl | Na2O | CO |
C | NaOH | NH3 | CaCl2 | MgO | SO2 |
D | KOH | HNO3 | CaCO3 | CaO | SO3 |
A. AB. BC. CD. D