题目内容
【题目】某研究小组制备84消毒液(主要成分NaClO)设计了如图装置。并查阅到下列资料:

Ⅰ.氯气与水的反应是放热反应;
Ⅱ.卤素单质与碱液发生反应:3X2+6OH-![]() 5X-+XO3-+3H2O。
5X-+XO3-+3H2O。
回答下列问题:
(1)装置中的大试管内发生反应的离子方程式为__。
(2)装置中能否省去盛饱和NaCl溶液的洗气瓶?__(填“能”或“不能”,下同),理由是__。
(3)装置中能否省去盛浓硫酸的洗气瓶?__,理由是__。
(4)装置中能否省去盛冰水的烧杯?__,理由是__。
【答案】Cl2+2OH-=Cl-+ClO-+H2O 不能 氯气中混有的HCl气体进入大试管中也会和氢氧化钠溶液反应,降低了NaClO的产量和纯度 能 少量水蒸气进入试管中不影响反应 不能 氯气与水的反应是放热反应,反应时温度升高,可能引起副反应,生成NaClO3
【解析】
装置分别是氯气的制备、净化、干燥和次氯酸钠的制备,结合物质的性质、装置特点和已知信息分析解答。
(1)氯气与氢氧化钠在冰水浴条件下反应生成氯化钠和次氯酸钠,反应的离子方程式Cl2+2OH-=Cl-+ClO-+H2O;
故答案为:Cl2+2OH-=Cl-+ClO-+H2O;
(2)浓盐酸易挥发,制取的氯气中含有氯化氢,用饱和食盐水除去氯化氢,否则氯化氢能与氢氧化钠溶液反应生成氯化钠,影响产品的产量和纯度,所以盛饱和氯化钠溶液的洗气瓶不能省略;
故答案为:不能;氯气中混有的氯化钠气体进入试管中也会和氢氧化钠溶液反应,降低了次氯酸钠的产量和纯度;
(3)氢氧化钠溶液中含有水,所以该实验不需要干燥氯气,可以将盛浓硫酸的洗气瓶省去,对实验不产生影响;
故答案为:能;少量水蒸气进入试管中不影响反应;
(4)依据题意可知,温度较高时,氯气与氢氧化钠反应生成氯酸钠,为防止副反应发生,盛冰水的烧杯不能省去;
故答案为:不能;氯气和水的反应是放热反应,反应时温度升高,可能会引起副反应,生成NaClO3。

【题目】I.反应![]() Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)![]() Fe(s)+CO2(g)H<0,在1000℃的平衡常数等于4.0.在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过10min后达到平衡.
Fe(s)+CO2(g)H<0,在1000℃的平衡常数等于4.0.在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过10min后达到平衡.
(1)CO的平衡转化率= ______ 。
(2)欲提高CO的平衡转化率,促进Fe2O3的转化,可采取的措施是 ______
a.提高反应温度 b.增大反应体系的压强
c.选取合适的催化剂 d.及时吸收或移出部分CO2
e.粉碎矿石,使其与平衡混合气体充分接触
II.(1)高炉炼铁产生的废气中的CO可进行回收,使其在一定条件下和H2反应制备甲醇: CO(g)+2H2(g)CH3OH(g)。请根据图示回答下列问题:
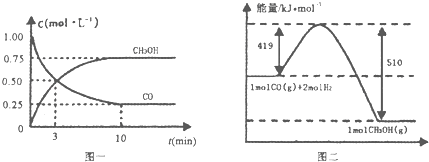
(1)从反应开始到平衡,用H2浓度变化表示平均反应速率v(H2)= ______ 。
(2)若在温度和容积相同的三个密闭容器中,按不同方式投入反应物,测得反应达到平衡吋的有关数据如下表:
容器 | 反应物投入的量 | 反应物的转化率 | CH3OH的浓度 | 能量变化 (Q1,Q2,Q3均大于0) |
甲 | 1molCO和2molH2 | a1 | c1 | 放出Q1kJ热量 |
乙 | 1molCH3OH | a2 | c2 | 吸收Q2kJ热量 |
丙 | 2molCO和4molH2 | a3 | c3 | 放出Q3kJ热量 |
则下列关系正确的是 ______ .
A c1=c2 B 2Q1=Q3 C 2a1=a3 D a1+a2=1 E 该反应若生成1molCH3OH,则放出(Q1+Q2)kJ热量。