题目内容
1.制纯碱包括石灰石分解、粗盐水精制、氨盐水碳酸化等基本步骤.完成下列计算:
(1)CaCO3质量分数为0.90的石灰石100kg完全分解产生CO220160L(标准状况).
石灰窑中,该石灰石100kg与焦炭混合焙烧,产生CO2 29120L(标准状况),如果石灰石中碳酸钙完全分解,且焦炭完全燃烧,不产生CO,则焦炭的物质的量为400mol.
(2)已知粗盐水含MgCl2 6.80mol/m3,含CaCl2 3.00mol/m3.
向粗盐水中加入Ca(OH)2除镁离子:MgCl2+Ca(OH)2→Mg(OH)2↓+CaCl2
然后加入Na2CO3除钙离子.
处理上述粗盐水10m3,至少需要加Na2CO310388g.
如果用碳酸化尾气(含NH3体积分数为0.100、CO2体积分数0.040)代替碳酸钠,发生如下反应:
Ca2++2NH3+CO2+H2O→CaCO3↓+2NH4+
处理上述10m3粗盐水至少需要通入多少L(标准状况)碳酸化尾气?列式计算.
(3)某氨盐水含氯化钠1521kg,通入二氧化碳后析出碳酸氢钠晶体,过滤后溶液中含氯化铵1070kg.列式计算:
①过滤后溶液中氯化钠的质量.
②析出的碳酸氢钠晶体的质量.
分析 (1)根据质量分数计算碳酸钙的质量,再根据CaCO3$\frac{\underline{\;\;△\;\;}}{\;}$CaO+CO2↑计算二氧化碳的体积;
碳酸钙分解产生二氧化碳,焦炭完全燃烧也生成二氧化碳,根据碳元素守恒计算焦炭的物质的量;
(2)加入碳酸钠最少时,反应完毕为NaCl溶液,反应过程中氯离子物质的量不变,根据氯离子守恒:n生成(NaCl)=2n(MgCl2)+2n(CaCl2 ),根据钠离子守恒:n生成(NaCl)=2n(Na2CO3 ),再根据m=nM计算Na2CO3 的质量;
加入的碳酸钠除钙离子,溶液中n(Ca2+)=n(Na2CO3),反应中NH3、CO2按物质的量之比2:1反应,而碳酸化尾气中NH3、CO2的物质的量之比为0.1:0.04=2.5:1,故反应中氨气有剩余,根据钙离子物质的量计算二氧化碳的物质的量,结合二氧化碳的体积分数计算碳酸化尾气的体积;
(3)①根据氯离子守恒计算滤液中NaCl物质的量,再根据m=nM计算;
②根据钠离子守恒计算生成碳酸氢钠的物质的量,再根据m=nM计算.
解答 解:(1)碳酸钙的质量为0.90×100kg=90Kg,即质量为90000g,设生成二氧化碳的体积为V,则:
CaCO3$\frac{\underline{\;\;△\;\;}}{\;}$CaO+CO2↑
100g 22.4
90000g V
所以V=$\frac{90000g×22.4L}{100g}$=20160L;
碳酸钙分解产生二氧化碳,焦炭完全燃烧也生成二氧化碳,根据碳元素守恒,焦炭燃烧生成的二氧化碳为29120L-20160L=8960L,焦炭与其燃烧生成的二氧化碳物质的量相等,故需要焦炭的物质的量为$\frac{8960L}{22.4L/mol}$=400mol,
故答案为:20160;400;
(2)加入碳酸钠最少时,反应完毕为NaCl溶液,反应过程中氯离子物质的量不变,
根据氯离子守恒:n生成(NaCl)=2n(MgCl2)+2n(CaCl2 )=10m3×6.80mol/m3×2+10m3×3.00mol/m3×2=196mol,根据钠离子守恒:n生成(NaCl)=2n(Na2CO3 ),故n(Na2CO3 )=$\frac{196mol}{2}$=98mol,故需要Na2CO3 的最少质量为98mol×106g/mol=10388g;
加入的碳酸钠除钙离子,溶液中n(Ca2+)=n(Na2CO3)=98mol,反应中NH3、CO2按物质的量之比2:1反应,而碳酸化尾气中NH3、CO2的物质的量之比为0.1:0.04=2.5:1,故反应中氨气有剩余,根据Ca2++2NH3+CO2+H2O→CaCO3↓+2NH4+,可知需要二氧化碳为98mol,故需要碳酸化尾气的体积为98mol×22.4L/mol÷0.04=54880L,
故答案为:10388;54880L;
(3)反应方程式为:NaCl(饱和)+NH3+H2O+CO2=NH4Cl+NaHCO3↓,
①原溶液中氯化钠的物质的量为$\frac{1521×1000g}{58.5g/mol}$=26×1000mol,滤液中氯化铵的物质的量为$\frac{1070×1000g}{53.5g/mol}$=20×1000mol,根据氯离子守恒,滤液中NaCl物质的量为26×1000mol-20×1000mol=6×1000mol,则过滤后溶液中氯化钠的质量为6×1000mol×58.5g/mol=351×1000g,即为351kg,
答:过滤后溶液中氯化钠的质量为351kg;
②根据钠离子守恒,生成碳酸氢钠的物质的量为26×1000mol-6×1000mol=20×1000mol,则析出碳酸氢钠的质量为20×1000mol×84g/mol=1680×1000g,即为1680kg,
答:析出碳酸氢钠的质量为1680kg.
点评 本题考查混合物的有关计算,注意利用守恒法进行计算解答,侧重考查学生的分析计算能力,题目过程复杂、计算量大,为易错题目,难度中等.

 科学实验活动册系列答案
科学实验活动册系列答案 如图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是( )
如图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是( )①C ②H2O2 ③Al ④Fe ⑤HNO3 ⑥H2S.
| A. | ①②③④ | B. | ②④⑤⑥ | C. | ①③⑤⑥ | D. | 全部 |
| A. | CH3CH2CH2CH2OH | B. |  | C. | 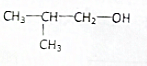 | D. | 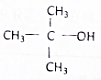 |
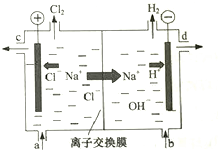 氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品.下图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过.
氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品.下图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过.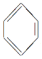 ; ④ CH3CH3。
; ④ CH3CH3。 H2CO3
H2CO3