题目内容
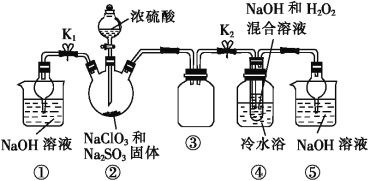
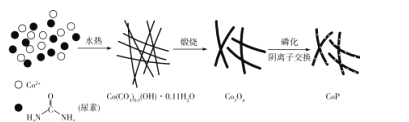
【题目】纳米磷化钴(CoP)常用于制作特种钻玻璃,制备磷化钴的常用流程如下:
(l)基态P原子的价电子排布式为____,P位于元素周期表中____区。
(2)尿素中N原子的杂化类型是 _____;C、N、O三种元素的第一电离能最大的是____,电负性由小到大的顺序为____。
(3)Co(CO3)0.5(OH)·0.11H2O中CO32-中C的价层电子对数为____;该化合物中不含有的化学键有_____填标号)。
A 离子键 B 共价键 C 金属键 D 配位键 E 氢键 F 非极性键
(4)一些氧化物的熔点如下表所示:
![]()
解释表中氧化物之间熔点差异的原因____。
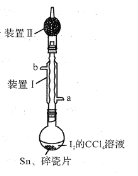
(5)CoP的晶胞结构如图所示,最近且相邻两个钴原子的距离为npm。
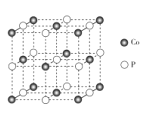
设NA为阿伏加德罗常数的值,则其晶胞密度为_______-g.cm-3(列出计算式即可)。
【答案】3s23p3 P sp3 N C<N<O 3 CF FeCl3是共价化合物,Fe3O4、Co3O4是离子化合物,Fe3O4、Co3O4晶胞结构不同 ![]()
【解析】
(l)P是15号元素,最外层有5个电子;
(2)根据尿素的结构简式是![]() 分析N原子杂化类型;同周期元素从左到右第一电离能增大,N原子3p轨道为半充满状态;同周期元素从左到右电负性依次增大;
分析N原子杂化类型;同周期元素从左到右第一电离能增大,N原子3p轨道为半充满状态;同周期元素从左到右电负性依次增大;
(3)CO32-中C的价层电子对数为![]() ;
;
(4)化合物类型不同熔沸点不同;晶体结构不同,熔沸点不同;
(5)根据CoP的晶胞结构,最近且相邻两个钴原子的距离为npm,则晶胞面对角线是2npm,晶胞的边长为![]() pm,1个晶胞含有Co原子数
pm,1个晶胞含有Co原子数![]() 、P原子数
、P原子数![]() ;
;
(l)P是15号元素,最外层有5个电子,基态P原子的价电子排布式为3s23p3;价电子排布式为3s23p3,所以P位于元素周期表中P区;
(2)尿素的结构简式是![]() ,N原子形成3个共价键,有1对孤电子对,所以N原子杂化类型是sp3;同周期元素从左到右第一电离能增大,N原子3p轨道为半充满状态,所以C、N、O三种元素的第一电离能最大的是N;同周期元素从左到右电负性依次增大,电负性由小到大的顺序为C<N<O;
,N原子形成3个共价键,有1对孤电子对,所以N原子杂化类型是sp3;同周期元素从左到右第一电离能增大,N原子3p轨道为半充满状态,所以C、N、O三种元素的第一电离能最大的是N;同周期元素从左到右电负性依次增大,电负性由小到大的顺序为C<N<O;
(3)CO32-中C的价层电子对数为![]() =3;
=3;
(4)FeCl3是共价化合物,熔沸点低;Fe3O4、Co3O4是离子化合物,熔沸点高,但晶胞结构不同,所以熔沸点有差异;Co(CO3)0.5(OH)·0.11H2O中CO32-与Co2+之间存在离子键;CO32-、水分子内存在共价键; Co2+与H2O是配位键;氢键不是化学键,没有非极性键,故选CF;
(5)根据CoP的晶胞结构,最近且相邻两个钴原子的距离为npm,则晶胞面对角线是2npm,晶胞的边长为![]() pm,晶胞体积为
pm,晶胞体积为![]() pm3,1个晶胞含有Co原子数
pm3,1个晶胞含有Co原子数![]() 、P原子数
、P原子数![]() ;所以晶胞密度为
;所以晶胞密度为![]() g.cm-3。
g.cm-3。