题目内容
【题目】下列有关说法不正确的是
A.C3H8中碳原子都采用的是sp3杂化
B.O2、CO2、N2都是非极性分子
C.酸性:H2CO3<H3PO4<H2SO4<HClO
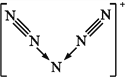
D.CO的一种等电子体为NO+,它的电子式为![]()
【答案】C
【解析】
A.C3H8分子中每个C原子含有4个δ键,所以每个C原子价层电子对个数是4,则C原子采用sp3杂化,故A正确;
B.O2、N2都是以非极性键结合的双原子分子一定为非极性分子,CO2中含有极性键,为直线形分子,结构对称,分子中正负电荷重心重叠,为非极性分子,故B正确;
C.非金属性:C<P<S<Cl,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,HClO不是氯元素的最高价氧化物对应的水化物,则酸性:H2CO3<H3PO4<H2SO4<HClO4,又H2CO3酸性大于HClO,则有酸性:HClO <H2CO3<H3PO4<H2SO4<HClO4,故C错误;
D.根据等电子体的定义,CO的等电子体必须是双原子分子或离子,且电子总数相等,如果是阳离子离子,原子序数之和减去所带电荷数值等于电子数,如:NO+它的电子式为![]() ,故D正确;
,故D正确;
综上所述,答案为C。

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目