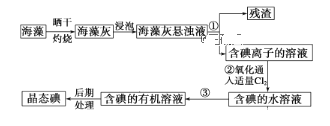
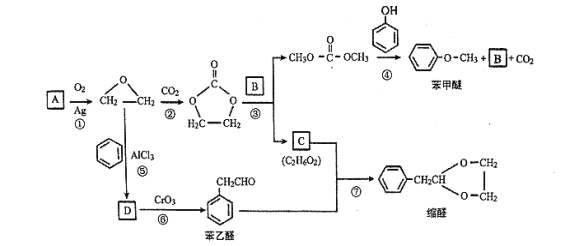
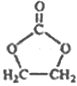
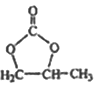
ЬтФПФкШн
ЁОЬтФПЁПМзДМЪЧвЛжжПЩдйЩњФмдДЃЌОпгаЙуЗКЕФПЊЗЂКЭгІгУЧАОАЁЃ
ЃЈ1ЃЉЙЄвЕЩЯвЛАуВЩгУЯТСаСНжжЗДгІКЯГЩМзДМЃК
ЗДгІЂёЃК CO(g) + 2H2(g) ![]() CH3OH(g) ІЄH1
CH3OH(g) ІЄH1
ЗДгІЂђЃК CO2(g) + 3H2(g) ![]() CH3OH(g) + H2O(g) ІЄH2
CH3OH(g) + H2O(g) ІЄH2
ЂйЯТБэЫљСаЪ§ОнЪЧЗДгІЂёдкВЛЭЌЮТЖШЯТЕФЛЏбЇЦНКтГЃЪ§ЃЈKЃЉЁЃ
ЮТЖШ | 250Ёц | 300Ёц | 350Ёц |
K | 2.041 | 0.270 | 0.012 |
гЩБэжаЪ§ОнХаЖЯІЄH1____0 ЃЈЬюЁАЃОЁБЁЂЁАЃНЁБЛђЁАЃМЁБЃЉЁЃ
Ђк ФГЮТЖШЯТЃЌНЋ2mol COКЭ6 mol H2ГфШы2LЕФУмБеШнЦїжаЃЌГфЗжЗДгІЃЌДяЕНЦНКтКѓЃЌВтЕУc(CO)ЃН 0.2 molЃЏLЃЌдђCOЕФзЊЛЏТЪЮЊ___________ЃЌДЫЪБЕФЮТЖШЮЊ_______ЃЈДгЩЯБэжабЁдёЃЉЁЃ
ЃЈ2ЃЉвбжЊдкГЃЮТГЃбЙЯТЃК
Ђй 2CH3OH(l) + 3O2(g) ЃН 2CO2(g) + 4H2O(l) ІЄH1ЃНЃ1451.6kJЃЏmol
Ђк 2CO (g)+ O2(g) ЃН 2CO2(g) ІЄH2 ЃНЃ566.0kJЃЏmol
аДГіМзДМВЛЭъШЋШМЩеЩњГЩвЛбѕЛЏЬМКЭвКЬЌЫЎЕФШШЛЏбЇЗНГЬЪНЃК_________________________________________
ЃЈ3ЃЉФГЪЕбщаЁзщвРОнМзДМШМЩеЕФЗДгІдРэЃЌЩшМЦШчЭМЫљЪОЕФЕчГизАжУЃК

ЂйИУЕчГиЕФФмСПзЊЛЏаЮЪНЮЊ___________________________ЁЃ
ЂкЙЄзївЛЖЮЪБМфКѓЃЌВтЕУШмвКЕФpHМѕаЁЁЃЧыаДГіИУЕчГиЕФИКМЋЕФЕчМЋЗДгІЪНЁЃ_____________________________
ЂлгУИУЕчГиЕчНтЃЈЖшадЕчМЋЃЉ500mLФГCuSO4ШмвКЃЌЕчНтвЛЖЮЪБМфКѓЃЌЮЊЪЙЕчНтжЪШмвКЛжИДЕНдзДЬЌЃЌашвЊЯђШмвКжаМгШы9.8g Cu(OH)2ЙЬЬхЁЃдђдCuSO4ШмвКЕФЮяжЪЕФСПХЈЖШЮЊ___________mol/LЃЈМйЩшЕчНтЧАКѓШмвКЬхЛ§ВЛБфЃЉЁЃ
ЁОД№АИЁП< 80% 250Ёц CH3OH(l)+O2(g) =CO(g)+2H2O(l) ЁїH= - 442.8kJ/mol ЛЏбЇФмзЊЛЏЮЊЕчФм CH3OHЃ6e-+ 8OH- = CO32- + 6H2O 0.2 mol/L
ЁОНтЮіЁП
ЃЈ1ЃЉЂйгЩБэжаЪ§ОнПЩжЊЃЌЩ§ИпЮТЖШKМѕаЁЃЌдђЛЏбЇЦНКтФцЯђвЦЖЏЃЌФцЗДгІЮЊЮќШШЗДгІЃЌЫљвде§ЗДгІЪЧЗХШШЗДгІЁЃЙЪЁїH1 <0ЃЛ
ЂкДяЕНЦНКтЪБВтЕУcЃЈCOЃЉ=0.2mol/LЃЌдђЯћКФCOЪЧ2molЃ0.2mol/LЁС2LЃН1.6molЃЌЫљвдCOЕФзЊЛЏТЪЪЧ![]() ЁС100ЃЅЃН80ЃЅЁЃЦНКтЪБЧтЦјЕФХЈЖШЪЧ1.4mol/LЃЌМзДМЪЧ0.8mol/LЃЌЫљвдДЫЪБK=
ЁС100ЃЅЃН80ЃЅЁЃЦНКтЪБЧтЦјЕФХЈЖШЪЧ1.4mol/LЃЌМзДМЪЧ0.8mol/LЃЌЫљвдДЫЪБK=![]() =2.041ЃЌвђДЫЮТЖШЪЧ250ЁцЃЛЃЈ2ЃЉвбжЊЂй 2CH3OH(l) + 3O2(g) ЃН 2CO2(g) + 4H2O(l) ІЄH1ЃНЃ1451.6kJЃЏmolЃЛЂк 2CO (g)+ O2(g) ЃН 2CO2(g) ІЄH2 ЃНЃ566.0kJЃЏmolЃЛИљОнИЧЫЙЖЈТЩЃКгЩЂйЁС
=2.041ЃЌвђДЫЮТЖШЪЧ250ЁцЃЛЃЈ2ЃЉвбжЊЂй 2CH3OH(l) + 3O2(g) ЃН 2CO2(g) + 4H2O(l) ІЄH1ЃНЃ1451.6kJЃЏmolЃЛЂк 2CO (g)+ O2(g) ЃН 2CO2(g) ІЄH2 ЃНЃ566.0kJЃЏmolЃЛИљОнИЧЫЙЖЈТЩЃКгЩЂйЁС![]() ЁЊЂкЁС
ЁЊЂкЁС![]() ЕУМзДМВЛЭъШЋШМЩеЩњГЩвЛбѕЛЏЬМКЭвКЬЌЫЎЕФШШЛЏбЇЗНГЬЪНЮЊЃКCH3OH(l)+O2(g) =CO(g)+2H2O(l) ЁїH=ІЄH1ЁС
ЕУМзДМВЛЭъШЋШМЩеЩњГЩвЛбѕЛЏЬМКЭвКЬЌЫЎЕФШШЛЏбЇЗНГЬЪНЮЊЃКCH3OH(l)+O2(g) =CO(g)+2H2O(l) ЁїH=ІЄH1ЁС![]() ЁЊІЄH2ЁС
ЁЊІЄH2ЁС![]() =Ѓ1451.6kJЃЏmolЁС
=Ѓ1451.6kJЃЏmolЁС![]() ЁЊЃЈЃ566.0kJЃЏmolЃЉЁС
ЁЊЃЈЃ566.0kJЃЏmolЃЉЁС![]() = - 442.8kJ/molЃЛЃЈ3ЃЉЂйМзЭщШМЩеЕчГиЪЧдЕчГиЃЌНЋЛЏбЇФмзЊЛЏЮЊЕчФмЃЛЂкМюадЬѕМўЯТЃЌЕчГиИКМЋЩЯМзДМЪЇЕчзгЗЂЩњбѕЛЏЗДгІЩњГЩЬМЫсИљРызгЃЌЕчМЋЗДгІЪНЮЊ ЃКCH3OHЃ6e-+ 8OH- = CO32- + 6H2OЃЛЂлМгШы9.8g CuЃЈOHЃЉ2ЙЬЬхФмЪЙЕчНтжЪШмвКЛжИДдзДЃЌn[CuЃЈOHЃЉ2]=
= - 442.8kJ/molЃЛЃЈ3ЃЉЂйМзЭщШМЩеЕчГиЪЧдЕчГиЃЌНЋЛЏбЇФмзЊЛЏЮЊЕчФмЃЛЂкМюадЬѕМўЯТЃЌЕчГиИКМЋЩЯМзДМЪЇЕчзгЗЂЩњбѕЛЏЗДгІЩњГЩЬМЫсИљРызгЃЌЕчМЋЗДгІЪНЮЊ ЃКCH3OHЃ6e-+ 8OH- = CO32- + 6H2OЃЛЂлМгШы9.8g CuЃЈOHЃЉ2ЙЬЬхФмЪЙЕчНтжЪШмвКЛжИДдзДЃЌn[CuЃЈOHЃЉ2]=![]() =0.1molЃЌЯрЕБгкМгШы0.1molCuOКЭ0.1molH2OЃЌИљОнCuдзгЪиКуЕУnЃЈCuSO4ЃЉ=n[CuЃЈOHЃЉ2]=0.1molЃЌдђcЃЈCuSO4ЃЉ=
=0.1molЃЌЯрЕБгкМгШы0.1molCuOКЭ0.1molH2OЃЌИљОнCuдзгЪиКуЕУnЃЈCuSO4ЃЉ=n[CuЃЈOHЃЉ2]=0.1molЃЌдђcЃЈCuSO4ЃЉ=![]() =0.2mol/LЁЃ
=0.2mol/LЁЃ

 дФЖСПьГЕЯЕСаД№АИ
дФЖСПьГЕЯЕСаД№АИЁОЬтФПЁПНќФъРДЁАЮэіВЁБЮлШОШевцбЯжиЃЌдвђжЎвЛЪЧЛњЖЏГЕЮВЦјжаКЌгаNOЁЂNO2ЁЂCOЕШЦјЬхЃЌЛ№СІЗЂЕчГЇЪЭЗХГіДѓСПЕФNOxЁЂSO2КЭCO2ЕШЦјЬхвВЪЧЦфдвђЃЌЯждкЖдЦфжаЕФвЛаЉЦјЬхНјааСЫвЛЖЈЕФбаОПЃК
ЃЈ1ЃЉгУ CH4ДпЛЏЛЙдЕЊбѕЛЏЮяПЩвдЯћГ§ЕЊбѕЛЏЮяЕФЮлШОЁЃ
вбжЊЃКЂйCH4(g) + 4NO2(g) = 4NO(g) + CO2(g) + 2H2O(g) ЁїH = - 574 kJ/mol
ЂкCH4(g) + 4NO(g) = 2N2(g) + CO2(g) + 2H2O(g) ЁїH = - 1160 kJ/mol
ЂлH2O(g) = H2O(l) ЁїH = - 44.0 kJ/mol
аДГі CH4(g)гы NO2(g)ЗДгІЩњГЩ N2(g)ЁЂCO2(g)КЭ H2O(l)ЕФШШЛЏбЇЗНГЬЪНЃК _____________________________________________________________ЁЃ
ЃЈ2ЃЉЦћГЕЮВЦјжаКЌгаCOЁЂNO2ЕШгаЖОЦјЬхЃЌЖдЦћГЕМгзАЮВЦјОЛЛЏзАжУЃЌПЩЪЙгаЖОЦјЬхзЊЛЏЮЊЮоЖОЦјЬхЁЃ4CO(g)ЃЋ2NO2(g) ![]() 4CO2(g)ЃЋN2(g) ІЄHЃН-1200 kJЁЄmol-1
4CO2(g)ЃЋN2(g) ІЄHЃН-1200 kJЁЄmol-1
ЖдгкИУЗДгІЃЌЮТЖШВЛЭЌЃЈT2ЃОT1ЃЉЁЂЦфЫћЬѕМўЯрЭЌЪБЃЌЯТСаЭМЯёе§ШЗЕФЪЧ________________ЃЈЬюДњКХЃЉЁЃ

ЃЈ3ЃЉгУЛюадЬПЛЙдЗЈвВПЩвдДІРэЕЊбѕЛЏЮяЃЌФГбаОПаЁзщЯђФГУмБеШнЦїМгШывЛЖЈСПЕФЛюадЬПКЭNOЃЌЗЂЩњЗДгІC(s)+2NO(g) ![]() N2(g)+CO2(g) ІЄH=a kJ/mol
N2(g)+CO2(g) ІЄH=a kJ/mol
дкT1ЁцЪБЃЌЗДгІНјааЕНВЛЭЌЪБМфВтЕУИїЮяжЪЕФСПХЈЖШШчЯТЃК
ЪБМф/min ХЈЖШ/(mol/L) | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.0 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
ЂйИљОнЭМБэЪ§ОнЗжЮіT1ЁцЪБЃЌИУЗДгІдк0-20minЕФЦНОљЗДгІЫйТЪvЃЈNOЃЉ=_____________________ЃЛМЦЫуИУЗДгІЕФЦНКтГЃЪ§K=____________________ЁЃ
Ђк30minКѓЃЌжЛИФБфФГвЛЬѕМўЃЌИљОнЩЯБэЕФЪ§ОнХаЖЯИФБфЕФЬѕМўПЩФмЪЧ_________ЃЈЬюзжФИДњКХЃЉЁЃ
AЃЎЭЈШывЛЖЈСПЕФCO2 BЃЎМгШыКЯЪЪЕФДпЛЏМС
CЃЎЪЪЕБЫѕаЁШнЦїЕФЬхЛ§ DЃЎЭЈШывЛЖЈСПЕФNO
EЃЎМгШывЛЖЈСПЕФЛюадЬП
ЂлШє30minКѓЩ§ИпЮТЖШжСT2ЁцЃЌДяЕНЦНКтЪБЃЌШнЦїжаNOЁЂN2ЁЂCO2ЕФХЈЖШжЎБШЮЊ2:1:1ЃЌдђДяЕНаТЦНКтЪБNOЕФзЊЛЏТЪ____________ЃЈЬюЁАЩ§ИпЁБЛђЁАНЕЕЭЁБЃЉЃЌa________0ЃЈЬюЁА>ЁБЛђЁА<ЁБЃЉЁЃ
ЃЈ4ЃЉЮТЖШT1КЭT2ЪБЃЌЗжБ№НЋ0.50 mol CH4КЭ1.2mol NO2ГфШы1 LЕФУмБеШнЦїжаЗЂЩњЗДгІЃКCH4(g)ЃЋ2NO2(g)![]() N2(g)ЃЋCO2(g)ЃЋ2H2O(g) ЁїH=bkJ/molЁЃ
N2(g)ЃЋCO2(g)ЃЋ2H2O(g) ЁїH=bkJ/molЁЃ
ВтЕУгаЙиЪ§ОнШчЯТБэЃК
ЮТЖШ | ЪБМф/min ЮяжЪЕФСП | 0 | 10 | 20 | 40 | 50 |
T1 | nЃЈCH4ЃЉ/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | nЃЈCH4ЃЉ/mol | 0.50 | 0.30 | 0.18 | x | 0.15 |
ЯТСаЫЕЗЈе§ШЗЕФЪЧ__________________ЁЃ
AЃЎT1ЃОT2ЃЌЧвbЃО0
BЃЎЕБЮТЖШЮЊT2ЁЂЗДгІНјааЕН40 minЪБЃЌ xЃО0.15
CЃЎЮТЖШЮЊT2ЪБЃЌШєЯђЦНКтКѓЕФШнЦїжадйГфШы0.50 mol CH4КЭ1.2mol NO2ЃЌжиаТДяЕНЦНКтЪБЃЌnЃЈN2ЃЉ<0.70mol
DЃЎЮТЖШЮЊT1ЪБЃЌШєЦ№ЪМЪБЯђШнЦїжаГфШы0.50 mol CH4(g)ЁЂ0.50 molNO2(g)ЁЂ1.0 mol N2(g)ЁЂ2.0 molCO2(g)ЁЂ0.50molH2O(g)ЃЌЗДгІПЊЪМЪБЃЌІЭ(е§)ЃОІЭ(Фц)