题目内容
【题目】常温下,下列说法正确的是 ( )
A.向![]() 溶液中加入等浓度等体积的盐酸:
溶液中加入等浓度等体积的盐酸:![]() =
=![]() +
+![]()
![]()
B.![]() 溶液中:
溶液中:![]()
C.pH相同的①![]() 溶液、②
溶液、②![]() 溶液中
溶液中![]() :①<②
:①<②
D.pH=9的![]() 的
的![]() 的溶液中:
的溶液中:![]()
【答案】B
【解析】
A.碳酸钠溶液中加入等浓度等体积的盐酸反应生成碳酸氢钠溶液和氯化钠溶液,根据物料守恒,n(Na)=n(C)+n(Cl),c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3)+c(Cl-),故A错误;
B.![]() 溶液中存在电荷守恒:c(Na+)+c(H+)=c(HS-)+2c(S2-)+c(OH-),存在物料守恒:c(Na+)=c(H2S)+c(HS-)+c(S2-),所以有c(S2-)+c(OH-)=c(H+)+c(H2S),故B正确;
溶液中存在电荷守恒:c(Na+)+c(H+)=c(HS-)+2c(S2-)+c(OH-),存在物料守恒:c(Na+)=c(H2S)+c(HS-)+c(S2-),所以有c(S2-)+c(OH-)=c(H+)+c(H2S),故B正确;
C.次氯酸根离子的水解程度大于醋酸根离子的水解程度,pH相同的①CH3COONa溶液、②NaClO溶液,溶液的浓度①>②,因此pH相同的①CH3COONa溶液、②NaClO溶液中c(Na+):①>②,故C错误;
D.pH=9的0.1molL-1的NaHR溶液显碱性,说明HR-的水解程度大于HR-的电离程度,溶液中:c(H2R)>c(R2-),故D错误;
故选B。

 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
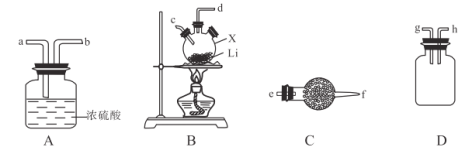
黄冈360度定制密卷系列答案【题目】用酸性KMnO4溶液与H2C2O4(草酸)溶液反应研究影响反应速率的因素,一实验小组欲通过测定单位时间内生成CO2的体积,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化),实验装置如图所示:
实验序号 | A溶液 | B溶液 |
① | 20mL 0.1mol·L-1H2C2O4溶液 | 30mL 0.01mol·L-1KMnO4溶液 |
② | 20mL 0.2mol·L-1H2C2O4溶液 | 30mL 0.01mol·L-1KMnO4溶液 |

(1)写出该反应的离子方程式__________________________________________。
(2)该实验探究的是________因素对化学反应速率的影响。相同时间内针筒中所得CO2的体积大小关系是______>______(填实验序号)。
(3)若实验①在2min末收集了4.48mL CO2(标准状况下),则在2min末,c(MnO4-)=______ mol·L-1(假设混合溶液的体积为50mL)。
(4)除通过测定一定时间内CO2的体积来比较反应速率外,本实验还可通过测定_________________________来比较化学反应速率。
(5)小组同学发现反应速率变化如图,其中t1-t2时间内速率变快的主要原因可能是:①反应放热,②___________________。

【题目】锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态Ge原子的核外电子排布式为[Ar]____,有____个未成对电子。
(2)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因________________________________。
GeCl4 | GeBr4 | GeI4 | |
熔点/℃ | -49.5 | 26 | 146 |
沸点/℃ | 83.1 | 186 | 约400 |
(3)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是____________。
(4)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为____,微粒之间存在的作用力是____。
(5)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置。如图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(1/2,0,1/2);C为(1/2,1/2,0)。则D原子的坐标参数为____。
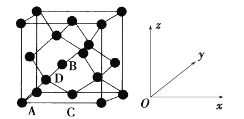
②晶胞参数,描述晶胞的大小和形状。已知Ge单晶的晶胞参数a pm,其密度为_________g·cm-3(列出计算式即可)。