题目内容
5.M(NO3)2的热分解化学方程式为:2M(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$2MO+4NO2↑+O2↑,加热29.6g M(NO3)2使其完全分解,在标准状况下收集2.24L的O2,则M的摩尔质量是24g/mol.分析 根据标准状况下的气体摩尔体积计算出气体的物质的量,再根据反应方程式中化学计量数关系计算出29.6g M(NO3)2的物质的量,根据M=$\frac{m}{n}$计算出摩尔质量,最后计算M的摩尔质量.
解答 解:在标准状况下收集气体体积为2.24L,物质的量为0.1mol,
根据反应方程式2M(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$2MO+4NO2↑+O2↑,
2 1
硝酸盐的物质的量为:0.1mol×2=0.2mol,M(NO3)2的摩尔质量为:$\frac{29.6g}{0.2mol}$=148g/mol,
摩尔质量在以g/mol为单位时,在数值上与相对分子量或相对原子量相等,所以M(NO3)2的式量为:148,M的相对原子量为:148-62×2=24,
所以M的摩尔质量为:24g/mol,
答:M的摩尔质量为24g/mol.
点评 本题考查了摩尔质量的计算,题目难度不大,要求熟练掌握物质的量与气体摩尔体积、摩尔质量之间的转化关系.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.在下列溶液中,各组离子一定能够大量共存的是( )
| A. | 无色溶液中:Na+、Cl、SO42-、Cu2+ | |
| B. | 使紫色石蕊溶液变红的溶液中:Na+、Ca2+、C032-、Cl- | |
| C. | 含SO42-的溶液中:K+、Ba2+、CI-、Br- | |
| D. | 酸性溶液中:Na+、S042-、Cl-、NH4+ |
17.已知:①C(s)+$\frac{1}{2}$O2(g)═CO(g)△H=-110.5kJ•mol-1
②H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8kJ•mol-1.
则制备水煤气的反应C(s)+H2O(g)═CO(g)+H2(g)的△H为( )
②H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8kJ•mol-1.
则制备水煤气的反应C(s)+H2O(g)═CO(g)+H2(g)的△H为( )
| A. | +262.6 kJ•mol-1 | B. | -131.3 kJ•mol-1 | C. | +131.3 kJ•mol-1 | D. | -352.3 kJ•mol-1 |
11.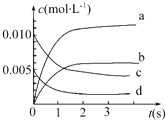 在2L密闭容器内,800℃时反应2NO(g)+O2(g)=2NO2(g)体系中,n(NO)随时间的变化如下表:
在2L密闭容器内,800℃时反应2NO(g)+O2(g)=2NO2(g)体系中,n(NO)随时间的变化如下表:
(1)上述反应是(填“是”或“不是”)可逆反应,在第5s时,NO的转化率为65%.
(2)如图中表示NO2变化曲线的是b.用O2表示0~2s内该反应的平均速率v=1.5×10-3mol•L-1•s-1.
(3)能说明该反应已达到平衡状态的是bc.
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(4)、铅蓄电池是常用的化学电源,其电极材料是Pb和PbO2,电解液为稀硫酸.工作时该电池总反应式为:PbO2+Pb+2H2SO4═2PbSO4+2H2O,据此判断:
①工作时正极反应为PbO2+4H++SO42-+2e-═PbSO4+2H2O.
②工作时,电解质溶液的pH值增大(“增大”、“减小”或“不变”)
③工作时,电解质溶液中阴离子移向负极.
(5)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水.当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热.已知0.4mol液态肼与足量液态双氧水反应,生成水蒸气和氮气,放出256.652kJ的热量.
①反应的热化学方程式为N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.63 kJ•mol-1.
②此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是产物不会造成环境污染.
③发射卫星可用肼为燃料,二氧化氮作氧化剂,两者反应生成氮气和水蒸气.已知:
N2(g)+2O2(g)═2NO2(g),△H=+67.7kJ•mol-1
N2H4(g)+O2(g)═N2(g)+2H2O(g),△H=-534kJ•mol-1
肼和二氧化氮反应的热化学方程式为N2H4(g)+NO2(g)═$\frac{3}{2}$N2(g)+2H2O(g)△H=-567.85 kJ•mol-1.
 在2L密闭容器内,800℃时反应2NO(g)+O2(g)=2NO2(g)体系中,n(NO)随时间的变化如下表:
在2L密闭容器内,800℃时反应2NO(g)+O2(g)=2NO2(g)体系中,n(NO)随时间的变化如下表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)如图中表示NO2变化曲线的是b.用O2表示0~2s内该反应的平均速率v=1.5×10-3mol•L-1•s-1.
(3)能说明该反应已达到平衡状态的是bc.
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(4)、铅蓄电池是常用的化学电源,其电极材料是Pb和PbO2,电解液为稀硫酸.工作时该电池总反应式为:PbO2+Pb+2H2SO4═2PbSO4+2H2O,据此判断:
①工作时正极反应为PbO2+4H++SO42-+2e-═PbSO4+2H2O.
②工作时,电解质溶液的pH值增大(“增大”、“减小”或“不变”)
③工作时,电解质溶液中阴离子移向负极.
(5)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水.当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热.已知0.4mol液态肼与足量液态双氧水反应,生成水蒸气和氮气,放出256.652kJ的热量.
①反应的热化学方程式为N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.63 kJ•mol-1.
②此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是产物不会造成环境污染.
③发射卫星可用肼为燃料,二氧化氮作氧化剂,两者反应生成氮气和水蒸气.已知:
N2(g)+2O2(g)═2NO2(g),△H=+67.7kJ•mol-1
N2H4(g)+O2(g)═N2(g)+2H2O(g),△H=-534kJ•mol-1
肼和二氧化氮反应的热化学方程式为N2H4(g)+NO2(g)═$\frac{3}{2}$N2(g)+2H2O(g)△H=-567.85 kJ•mol-1.