题目内容
15.工业上利用氨氧化获得的高浓度NOx气体(含NO、NO2)制备NaNO2、NaNO3,工艺流程如下: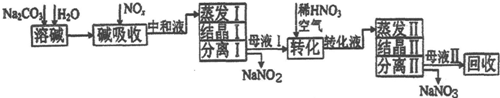
已知:Na2CO3+NO+NO2═2NaNO2+CO2
(1)氨氧化法获得NO、NO2气体的方程式分别为4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,2NO+O2=2NO2.
(2)中和液所含溶质除NaNO2及少量Na2CO3外,还有NaNO3 (填化学式).
(3)中和液进行蒸发I操作时,应控制水的蒸发量,避免浓度过大,目的是防止NaNO2的析出.蒸发I产生的蒸汽中含有少量NaNO2等有毒物质,不能直接排放,将其冷凝后用于流程中的一(填操作名称)最合理.
(4)在实验室里实现分离l的操作名称是过滤.母液II需回收利用,下列处理方法合理的是cd.
a.转入中和液 b.转入结晶I操作 c.转入转化液 d.转入结晶II操作
(5)若将NaNO2、NaNO3两种产品的物质的量之比设为2:1,则生产1.38吨NaNO2时,Na2CO3的理论用量为1.59吨(假设NaNO2恰好完全反应).
分析 由制备流程可知,碳酸钠溶解后,碱吸收发生Na2CO3+NO+NO2═2NaNO2+CO2、3NO2+H2O=HNO3+NO、Na2CO3+2HNO3=NaNO3+H2O+CO2↑,然后中和液进行蒸发Ⅰ操作,应避免浓度过大NaNO2析出,蒸发Ⅰ产生的蒸汽中含有少量的NaNO2等有毒物质要回收再循环利用;结晶过滤分离出NaNO3,母液I中主要含NaNO2,母液Ⅰ进行转化时加入稀HNO3、空气,硝酸提供酸性环境,可将NaNO2转化为NaNO3,转化液蒸发、结晶、过滤分离出NaNO3,母液Ⅱ中主要含NaNO3.
(1)氨气具有还原性,氧气具有氧化性,氨气中氮元素为-3价,被氧气氧化为+2价的氮元素,所以氨气和氧气反应生成一氧化氮和水,NO易与空气中的O2反应生成二氧化氮气体,据此分析解答;
(2)由上述分析可知,二氧化氮与碱液反应生成NaNO2,还可生成NaNO3,中和液中含剩余的少量Na2CO3,
(3)中和液进行蒸发Ⅰ操作时,应控制水的蒸发量,避免浓度过大,目的是防止NaNO2的析出,NaNO2等有毒要回收再循环利用;
(4)固液分离通常采用过滤的方法,母液Ⅱ需回收利用,可转入转化液或转入结晶Ⅱ操作,提高其利用率;
(5)生产1.38吨NaNO2时,n(NaNO2)=$\frac{1.38×1{0}^{6}g}{69g/mol}$=2×104mol,NaNO2、NaNO3两种产品的物质的量之比为2:1,则n(NaNO3)=1×104mol,由Na原子守恒可知,2n(Na2CO3)=n(NaNO2)+n(NaNO3),结合m=nM计算.
解答 解:(1)NH3与过量O2在催化剂、加热条件下发生反应生成一氧化氮和水,反应方程为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,
常温下NO易与空气中的O2反应生成红棕色的二氧化氮气体,2NO+O2=2NO2,
故答案为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;2NO+O2=2NO2;
(2)由制备流程可知,碳酸钠溶解后,碱吸收发生Na2CO3+NO+NO2═2NaNO2+CO2、3NO2+H2O=HNO3+NO、Na2CO3+2HNO3=NaNO3+H2O+CO2↑,所以中和液所含溶质除NaNO2及少量Na2CO3外,还有NaNO3,
故答案为:NaNO3;
(3)中和液进行蒸发Ⅰ操作时,应控制水的蒸发量,避免浓度过大,目的是防止NaNO2的析出,蒸发Ⅰ产生的蒸汽中含有少量的NaNO2等有毒物质,不能直接排放,将其冷凝后用于流程中的溶碱,循环利用,提高利用率,
故答案为:防止NaNO2的析出;溶碱;
(4)由上述分析可知,结晶过滤分离出NaNO3,母液I中主要含NaNO2,母液Ⅱ需回收利用,可转入转化液或转入结晶Ⅱ操作,提高其利用率,
故答案为:过滤;cd;
(5)生产1.38吨NaNO2时,n(NaNO2)=$\frac{1.38×1{0}^{6}g}{69g/mol}$=2×104mol,NaNO2、NaNO3两种产品的物质的量之比为2:1,则n(NaNO3)=1×104mol,由Na原子守恒可知,2n(Na2CO3)=n(NaNO2)+n(NaNO3),m(Na2CO3)=(2×104mol+1×104mol)×$\frac{1}{2}$×106g/mol=1.59×106g=1.59t,
故答案为:1.59.
点评 本题考查工业制备NaNO2、NaNO3,涉及物质的制备流程及混合物分离提纯综合应用,把握流程中的反应、分离方法为解答的关键,注意工业生产与环境保护、原料利用率等,侧重分析与应用能力的综合考查,题目难度中等.

 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案| A. | 烧菜用过的铁锅,经放置因发生氧化还原反应常出现红棕色斑迹 | |
| B. | 用过滤的方法除去NaCl溶液中含有的少量的MgSO4 | |
| C. | 蒸馏时温度计时用来测定蒸馏烧瓶中液体的温度 | |
| D. | 用加热、蒸发的方法可以除去NaCl中CaCl2、MgCl2等杂质 |
| A. | 硫酸的摩尔质量是98g | B. | 1mol N2的质量为28g/mol | ||
| C. | 摩尔是物质的量的单位 | D. | 1mol氧的质量等于16g |
| A. | 1.02 | B. | 1.68 | C. | 1.00 | D. | 0.986 |
| A. | H2SO4的摩尔质量是98 g•mol-1 | |
| B. | 2mol NO和2mol N2气体体积相等 | |
| C. | 等质量的O2和O3中所含氧原子个数相同 | |
| D. | 等物质的量的CO和CO2中所含碳原子数相等 |
| A. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl | B. | nCH2=CH2$\stackrel{一定条件}{→}$ | ||
| C. |  +HNO3$→_{加热}^{浓硫酸}$ +HNO3$→_{加热}^{浓硫酸}$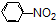 +H2O +H2O | D. | 2CH3CH2OH+2Na→2CH3CH2ONa+H2↑ |