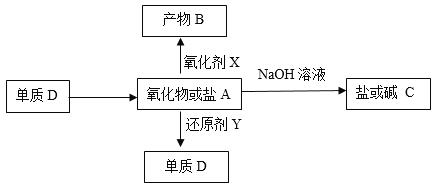
��Ŀ����
����Ŀ����ϩ�����ںϳ�ɱ�������߳��ũҩ������ʽΪC3H5Br2Cl����Ӧ�ù㷺��DAP��֬�� 
��֪���봼�ɷ���������������Ӧ��
RCOOR��+R��OH ![]() RCOOR��+R��OH ��R��R�䡢R�����������
RCOOR��+R��OH ��R��R�䡢R�����������
��1��ũҩ����C3H5Br2Cl��ÿ��̼ԭ���Ͼ�����±ԭ�ӣ� ��A�Ľṹ��ʽ�� �� A���еĹ�������������
���ɱ�ϩ����A�ķ�Ӧ������ ��
��2��Aˮ��ɵõ�D����ˮ�ⷴӦ�Ļ�ѧ����ʽ�� ��
��3��C�����ܶ�����ͬ״̬�¼����ܶȵ�6.25����C�и�Ԫ�ص����������ֱ�Ϊ��̼60%����8%����32%��C�Ľṹ��ʽ�� ��
��4������˵����ȷ���ǣ�ѡ�������ĸ�� �� a��C�ܷ����ۺϷ�Ӧ����ԭ��Ӧ��������Ӧ
b��C����2������������ͬ���칹����4��
c��D������IJ�����B������ͬ����Է�������
d��E���з�����ζ���������Ҵ�
��5��E��ˮ����ᆳ�������յõ��״���B�����߾���ѭ��������DAP��֬���Ʊ������н��״���H����IJ��������� ��
��6��F�ķ���ʽΪC10H10O4 �� DAP����Ϊ���Ķ�Ԫȡ���������ȡ���������ڶ�λ���õ��屽���ϵ�һ��ȡ����ֻ�����֣�D��F��Ӧ����DAP����Ļ�ѧ����ʽ�� ��
���𰸡�
��1��CH2=CHCH2Cl��̼̼˫������ԭ�ӣ�ȡ��
��2��CH2=CHCH2Cl+H2O ![]() HOCH2CH=CH2+HCl
HOCH2CH=CH2+HCl
��3��CH3COOCH2CH=CH2
��4��a c d
��5������
��6��![]()
���������⣺ũҩ����C3H5Br2Cl��ÿ��̼ԭ���Ͼ�����±ԭ�ӣ����֪��ϩ��500�������·���ȡ����Ӧ����
A��CH2=CHCH2Cl����A���巢���ӳɷ�Ӧ����C3H5Br2Cl��C�����ܶ�����ͬ״̬�¼����ܶȵ�6.25����C�и�Ԫ�ص����������ֱ�Ϊ��̼60%����8%����32%������Է�������Ϊ6.25��16=100�������к�N��C��= ![]() =5��N��H��=
=5��N��H��= ![]() =8��N��O��=
=8��N��O��= ![]() =2�������ʽΪC5H8O2��C�ܼ״�������������ӦΪ������ϩ��B��Ӧ���Եõ�C����C�Ľṹ��ʽΪCH3COOCH2CH=CH2��C��D������������Ӧ����DΪHOCH2CH=CH2��EΪCH3COOCH3��ˮ�����ɼ״���B����BΪCH3COOH��HΪCH3COONa����1���������Ϸ�����֪AΪCH2=CHCH2Cl������̼̼˫������ԭ�ӹ����ţ����Դ��ǣ�CH2=CHCH2Cl��̼̼˫������ԭ�ӣ�
=2�������ʽΪC5H8O2��C�ܼ״�������������ӦΪ������ϩ��B��Ӧ���Եõ�C����C�Ľṹ��ʽΪCH3COOCH2CH=CH2��C��D������������Ӧ����DΪHOCH2CH=CH2��EΪCH3COOCH3��ˮ�����ɼ״���B����BΪCH3COOH��HΪCH3COONa����1���������Ϸ�����֪AΪCH2=CHCH2Cl������̼̼˫������ԭ�ӹ����ţ����Դ��ǣ�CH2=CHCH2Cl��̼̼˫������ԭ�ӣ�
���ɱ�ϩ����A�ķ�Ӧ������ȡ�������Դ��ǣ�ȡ������2��Aˮ��ɵõ�D����ˮ�ⷴӦ�Ļ�ѧ����ʽΪCH2=CHCH2Cl+H2O ![]() HOCH2CH=CH2+HCl��
HOCH2CH=CH2+HCl��
���Դ��ǣ�CH2=CHCH2Cl+H2O ![]() HOCH2CH=CH2+HCl����3��C�����ܶ�����ͬ״̬�¼����ܶȵ�6.25����C�и�Ԫ�ص����������ֱ�Ϊ��̼60%����8%����32%������Է�������Ϊ6.25��16=100�������к�N��C��=
HOCH2CH=CH2+HCl����3��C�����ܶ�����ͬ״̬�¼����ܶȵ�6.25����C�и�Ԫ�ص����������ֱ�Ϊ��̼60%����8%����32%������Է�������Ϊ6.25��16=100�������к�N��C��= ![]() =5��N��H��=
=5��N��H��= ![]() =8��N��O��=
=8��N��O��= ![]() =2�������ʽΪC5H8O2��C�ܼ״�������������ӦΪ������ϩ��B��Ӧ���Եõ�C����C�Ľṹ��ʽΪCH3COOCH2CH=CH2��
=2�������ʽΪC5H8O2��C�ܼ״�������������ӦΪ������ϩ��B��Ӧ���Եõ�C����C�Ľṹ��ʽΪCH3COOCH2CH=CH2��
���Դ��ǣ�CH3COOCH2CH=CH2����4��a��CΪCH3COOCH2CH=CH2���ɷ����ۺϷ�Ӧ����ԭ��Ӧ��������Ӧ����a��ȷ��
b��C����2������������ͬ���칹����CH3C��CH3��=CH2COOH��CH3CH=C��CH3��COOH 2�֣���b����
c��DΪCH2=CHCH2OH���ӳɲ���ΪCH3CH2CH2OH����Է�������Ϊ60��BΪCH3COOH����Է�������Ϊ60����c��ȷ��
d��EΪCH3COOCH3�����з�����ζ���������Ҵ�����d��ȷ��
���Դ��ǣ�a c d����5��HΪ�����ƣ���״��ķе����ϴ���������ķ��������룬���Դ��ǣ�����6��F�ķ���ʽΪC10H10O4��DAP����Ϊ���Ķ�Ԫȡ���������ȡ���������ڶ�λ���õ��屽���ϵ�һ��ȡ����ֻ�����֣�Ӧλ����λ��DΪCH2=CHCH2OH����FΪ ![]() ����Ӧ����DAP����Ļ�ѧ����ʽ��
����Ӧ����DAP����Ļ�ѧ����ʽ�� ![]() ��
��
���Դ��ǣ� ![]() ��
��

����Ŀ��NH3��Ϊ��Ҫ����ԭ�ϣ�������Ӧ���ڹ�ҵ�����������й����ʷ�Ӧ�Ĵ����о������������863�ƻ���
��1�����Ĵ�������Ӧ:4 NH3��g��+5O2��g��![]() 4NO��g��+6H2O��g�� ��H< 0����������Ļ�����Ӧ�����ݻ��̶����ܱ������з���������Ӧ�������ڲ������ʵ����ʵ���Ũ�����±���
4NO��g��+6H2O��g�� ��H< 0����������Ļ�����Ӧ�����ݻ��̶����ܱ������з���������Ӧ�������ڲ������ʵ����ʵ���Ũ�����±���
Ũ�� ʱ�� | C(NH3) mol/L | C(O2) mol/L | C(NO) mol/L |
��0 min | 0.8 | 1.6 | 0 |
��1 min | a | 1.35 | 0.2 |
��2 min | 0.3 | 0.975 | 0.5 |
��3 min | 0.3 | 0.975 | 0.5 |
��4 min | 0.7 | 1.475 | 0.1 |
�ٷ�Ӧ�ڵ�1min����2minʱ��NH3��ƽ����Ӧ����Ϊ______________��
�ڷ�Ӧ�ڵ�3 minʱ�ı����������ı������������___________������ţ���
A��ʹ�ô��� B����Сѹǿ C�������¶� D������O2��Ũ��
��˵��4NH3��g��+5O2��g��![]() 4NO��g��+6 H2O��g���ﵽƽ��״̬����____������ţ���
4NO��g��+6 H2O��g���ﵽƽ��״̬����____������ţ���
A����λʱ��������n mol NO��ͬʱ����n mol NH3
B���ٷֺ���w��NH3��=w��NO��
C����Ӧ����v��NH3����v��O2����v��NO����v��H2O��=4��5��4��6
D���ں��º��ݵ������У���������ƽ����Է����������ٱ仯
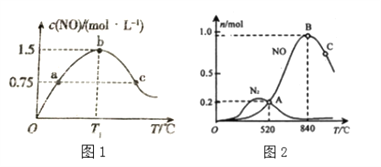
��2�������ݻ�Ϊ2L���ܱ������г���4.0molNH3(g)��5.0molO2(g)���������·�Ӧ��4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g)�����������������䣬����ͬ��ʱ���ڲ��c(NO)���¶ȵĹ�ϵ����ͼ1��ʾ���� T1���£�NH3��ƽ��ת����Ϊ______��
4NO(g)+6H2O(g)�����������������䣬����ͬ��ʱ���ڲ��c(NO)���¶ȵĹ�ϵ����ͼ1��ʾ���� T1���£�NH3��ƽ��ת����Ϊ______��
��3����������ʱ�ᷢ������������Ӧ���ֱ�Ϊ
��ӦI��4NH![]() 4NO(g) +6H2O(g) ��H= -905.0 kJ��mol-1
4NO(g) +6H2O(g) ��H= -905.0 kJ��mol-1
��ӦII: 4NH3(g)+3O2(g)![]() 2N2(g) +6H2O(g) ��H= -1266.6 kJ��mol-1��
2N2(g) +6H2O(g) ��H= -1266.6 kJ��mol-1��
Ϊ����ij�����Ը÷�Ӧ��ѡ���ԣ���1L�ܱ������г���1 mol NH3��2mol O2������й����ʵ�����ϵ����ͼ2��
�ٸô����ڵ���ʱѡ��Ӧ_______(� I ���� II������
��C���B����������NO�����ʵ����ٵ���Ҫԭ��______________________________����4��ͨ����������������Ӧд��NO�ֽ�����N2��O2���Ȼ�ѧ����ʽ________________��