题目内容
【题目】元素X的某价态离子Xn+中所有电子正好充满K、L、M三个电子层,它与N3-形成晶体的晶胞结构如图所示。下列说法错误的是( )
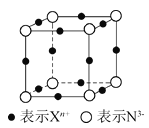
A.X元素的原子序数是19
B.该晶体中阳离子与阴离子个数比为3∶1
C.Xn+中n=1
D.晶体中每个Xn+周围有2个等距离且最近的N3-
【答案】A
【解析】
该晶胞中Xn+个数=12×![]() =3、N3-个数=8×
=3、N3-个数=8×![]() =1,所以N3-、Xn+个数之比为1∶3,根据化合价的代数和为0知n=+1,元素X的某价态离子Xn+中所有电子正好充满K、L、M三个电子层,则X原子核外电子数=2+8+18+1=29,为Cu元素,该化合物为Cu3N,据此分析解答。
=1,所以N3-、Xn+个数之比为1∶3,根据化合价的代数和为0知n=+1,元素X的某价态离子Xn+中所有电子正好充满K、L、M三个电子层,则X原子核外电子数=2+8+18+1=29,为Cu元素,该化合物为Cu3N,据此分析解答。
A.根据上述分析,X为Cu元素,核电荷数为29,故A错误;
B.该晶胞中Xn+个数=12×![]() =3、N3-个数=8×
=3、N3-个数=8×![]() =1,所以该晶体中阳离子与阴离子个数比为3∶1,故B正确;
=1,所以该晶体中阳离子与阴离子个数比为3∶1,故B正确;
C.N3-、Xn+个数之比为1∶3,根据化合物中化合价的代数和为0判断n=1,故C正确;
D.以一个棱上的Xn+为中心,该离子被4个晶胞共用,与晶体中每个Xn+周围等距离且最近的N3-只有其相邻顶点上的离子,有2个,故D正确;
故选A。

【题目】某校化学兴趣小组的同学用滴定法对一含有少量Na2SO4的NaOH样品中NaOH的含量进行测定,回答下列问题:
(1)用分析天平准确称取该样品5.0g,全部溶于水配制成1000.0mL的溶液。用____(填一仪器名称)量取其中20.00mL放在锥形瓶中,滴加几滴指示剂,待测。该中和滴定中可选用的指示剂是__________________________,(如有几种,可任填一种)滴定终点的现象是___________________________________________________________。
(2)用0.10mol/L的盐酸溶液滴定未知浓度的NaOH溶液,实验数据如下表所示,
实验编号 | 待测NaOH溶液的体积/mL | HCl溶液的体积/mL |
1 | 20.00 | 24.01 |
2 | 20.00 | 23.99 |
3 | 20.00 | 22.10 |
计算样品中,NaOH的质量百分含量为__________________。
(3)若滴定前,滴定管尖端有气泡,滴定终了气泡消失,将使所测结果______(填“偏高”、“偏低”或“不变”,下同),若读酸式滴定管读数时,滴定前仰视读数,滴定后正确读数,则所测结果_______;
(4)下图为0.10mol/L 25 mL NaOH溶液中逐滴滴加0.10mol/L CH3COOH溶液过程中溶液pH的变化曲线,请回答:
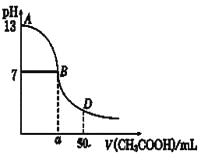
①B点溶液呈中性,有人据此认为,在B点时NaOH与CH3COOH恰好完全反应,这种看法是否正确?______(选填“是”或“否”)。若不正确,则二者恰好完全反应的点是在AB区间还是BD区间内?________区间。(若正确,此问不答)。
②在D点时,溶液中c(CH3COO-)+c(CH3COOH)______2c(Na+)。(填“>”、“<”或“=”)