题目内容
【题目】设NA为阿伏加德罗常数的值,下列说法不正确的是
A.1molFeI2与1molCl2反应时转移的电子数为2NA
B.25℃时,pH=3的醋酸溶液1 L,溶液中含H+的数目等于0.001 NA
C.标准状况下22.4L丙烷中含C-H键数约为8NA
D.18g 2H2O 中含有的质子数为10NA
【答案】D
【解析】
A.1molFeI2 与1molCl2 反应,氯气完全反应生成2mol氯离子,转移的电子数为2NA,故A正确;
B.25 °C时,pH=3的醋酸溶液1L,氢离子浓度为0.001mol/L,含有氢离子个数= 0.001mol/L![]() 1L
1L![]() NA/mol=0.001 NA,故B正确;
NA/mol=0.001 NA,故B正确;
C.1个丙烷分子含有8个C- H键,标准状况下22.4L丙烷中含C- H键数约为8NA,故C正确;
D.18g 2H2O 中含有的质子数=![]()
![]() 10
10![]() NA/mol=9NA,故D错误;
NA/mol=9NA,故D错误;
故答案:D。

练习册系列答案
相关题目
【题目】已知:①1mol晶体硅中含有2molSi—Si键。
②Si(s)+O2(g)===SiO2(g) ΔH,其反应过程与能量变化如图所示。
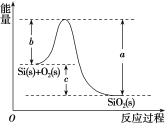
③
化学键 | Si—O | O=O | Si—Si |
断开1 mol共价键所需能量/kJ | 460 | 500 | 176 |
下列说法中正确的是( )
A.晶体硅光伏发电是将化学能转化为电能B.二氧化硅稳定性小于硅的稳定性
C.ΔH=-988kJ·mol-1D.ΔH=(a-c)kJ·mol-1