题目内容
14.有一化学反应:aA+bB?C,根据影响化学反应速率的因素可得v0=kcm(A)cn(B),其中k是与温度有关的常数,为测得k、m、n的值,在298K时,将A、B溶液按不同浓度混合,得到下表中的实验数据:| 编号 | A的初$\frac{始浓度}{mol•{L}^{-1}}$ | B的初$\frac{始浓度}{mol•{L}^{-1}}$ | 生成C的$\frac{初始速率}{mol•{L}^{-1}•{s}^{-1}}$ |
| 1 | 1.0 | 1.0 | 1.2×10-2 |
| 2 | 2.0 | 1.0 | 2.4×10-2 |
| 3 | 4.0 | 1.0 | 4.9×10-2 |
| 4 | 1.0 | 1.0 | 1.2×10-2 |
| 5 | 1.0 | 2.0 | 4.8×10-2 |
| 6 | 1.0 | 4.0 | 1.9×10-1 |
(2)若a=m,b=n,当c(A)=c(B)=2.0mol•L-1时,求以B表示的初始反应速率.
分析 (1)用B数据相同的两组,使A数据成倍数关系,即可求出m值(如选编号1、2两组);同样方法求出n值(如选编号1、5两组);将得到的m=1、n=2代入其中一组数据即可求出K,求得m、n、K值;
(2)利用方程式及反应速率表达式即可求出B的初始反应速率.
解答 解:(1)将1、2数据代入v0=kcm(A)cn(B)可得:$\left\{\begin{array}{l}{k×1.{0}^{m}×1.{0}^{n}=1.2×1{0}^{-2}}\\{k×2.{0}^{m}×1.{0}^{n}=2.4×1{0}^{-2}}\end{array}\right.$,解得m=1,
将表中1、5数据代入v0=K{c(A)}m•{c(B)}n可得:$\left\{\begin{array}{l}{k×1.{0}^{m}×1.{0}^{n}=1.2×1{0}^{-2}}\\{k×1.{0}^{m}×2.{0}^{n}=4.8×1{0}^{-2}}\end{array}\right.$,解得:n=2,
将m=1、n=2及数据1代入v0=kcm(A)cn(B)可得:K×1.01×1.02=1.2×10-2,解得K=1.2×10-2L2•mol-2•s-1,
故答案为:1;2;1.2×10-2;L2•mol-2•s-1;
(2)将(1)得出的m=1,n=2,K=1.2×10-2L2•mol-2•s-1和c(A)=c(B)=2.0 mol•L-1代入,v(C)=(1.2×10-2 L2•mol-2•s-1)×(2.0 mol•L-1)×(2.0 mol•L-1)2=9.6×10-2 mol•L-1•s-1,由于b=n=2,所以v(B)=2v(C)=9.6×10-2 mol•L-1•s-1×2=1.92×10-1mol•L-1•s-1,
故答案为:以B表示的初始反应速率为v(B)=1.92×10-1mol•L-1•s-1.
点评 本题考查了化学反应速率的计算,题目难度中等.注意熟练掌握化学反应速率的概念及表达式,试题侧重学生的分析、理解能力及灵活应用所学知识的能力的培养.

 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案| A. | N4的摩尔质量是56 g | |
| B. | N4与N2互为同位素 | |
| C. | 相同质量的N4和N2含原子个数比为1:2 | |
| D. | N4与N2互为同素异形体 |
| A. | c(K+)>c(NO3-)>c(Cl-)>c(Ag+)>c(I-) | B. | c(K+)>c(NO3-)>c(Ag+)>c(Cl-)>c(I-) | ||
| C. | c(NO3-)>c(K+)>c(Ag+)>c(Cl-)>c(I-) | D. | c(K+)>c(NO3-)>c(Ag+)=(Cl-)+c(I-) |
| A. | 溶液pH由大变小 | B. | 负极附近Zn2+浓度逐渐增大 | ||
| C. | H+向负极移动 | D. | 溶液中H2SO4的浓度不变 |
| A. |  铁丝的析氢腐蚀实验 | B. | 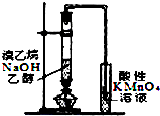 检验该反应的有机产物 | ||
| C. | 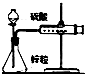 结合秒表测量锌与硫酸的反应速率 | D. | 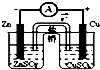 验证化学能转化为电能 |
| A. | NO和O2 | B. | NH3和HCl | C. | NH3和O2 | D. | H2S和SO2 |
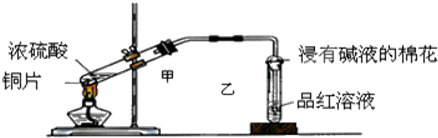
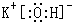 (填写电子式);
(填写电子式);